Секция «Стратегические решения терапии глаукомы
Профессор Н.И. Курышева (Москва) выступила с докладом «Стартовое патогенетически ориентированное лечение глаукомы». Большое внимание в докладе было уделено роли искусственного интеллекта (ИИ) в выявлении характера заболевания и определении методики лечения.
По результатам многолетних исследований разные формы глаукомы прогрессируют с разной скоростью, при это скорость прогрессирования может отличаться в 2-3 раза. Существуют несколько фенотипов, определяющих диагноз «глаукома»: GE – фенотип с генерализованно увеличенной экскавацией ДЗН; FI – фокально-ишемический фенотип; MY – миопический фенотип; SS – сенильно-склеротический фенотип.
Было показано, что для различных фенотипов характерны различные паттерны и скорость прогрессирования. К примеру, при миопическом фенотипе прогрессирование заболевания происходит крайне медленно; наиболее быстрое, выраженное и диффузное истончение характерно для склеротического типа; при фокальном происходит выраженное секторальное истончение.
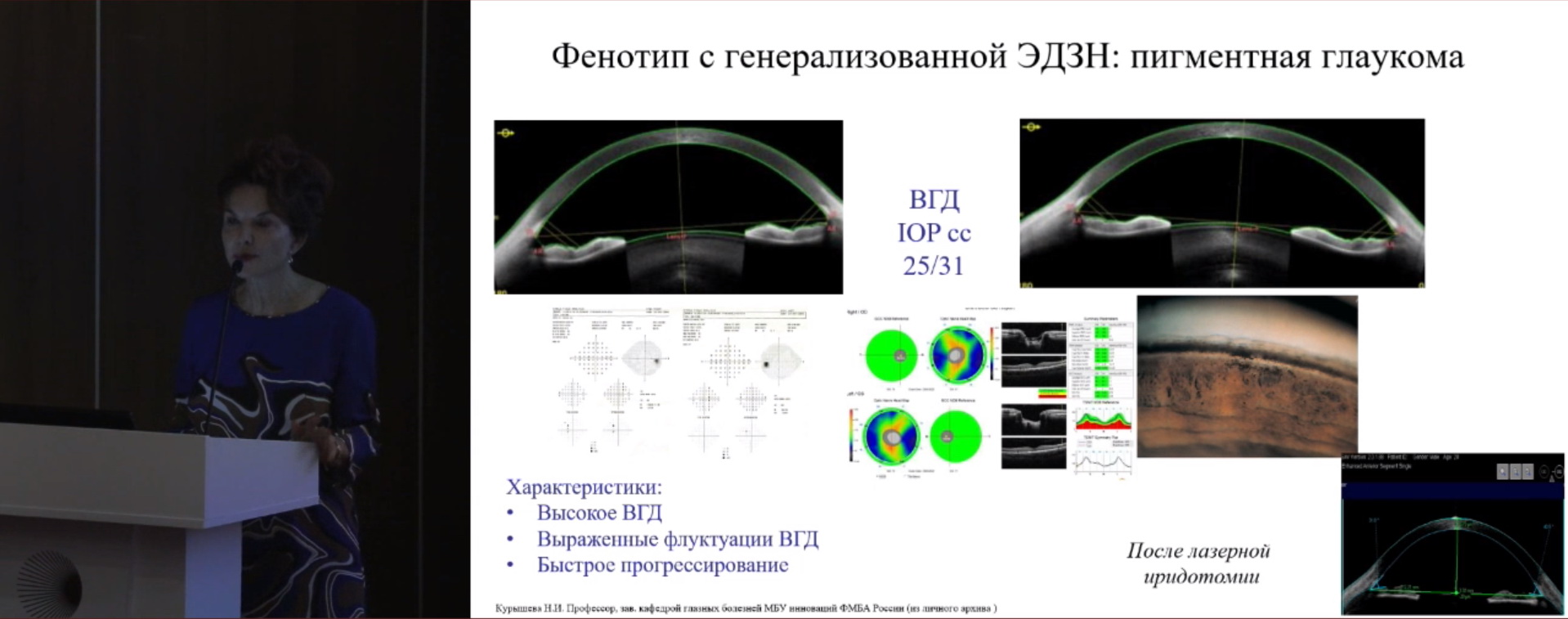
Ярким представителем фенотипа с генерализованной экскавацией ДЗН является пигментная глаукома (рис. 1) и ПЗУГ (рис. 2). При сканировании переднего отрезка глаза визуализируются гониосинехии, что подразумевает неэффективность лазерной иридэктомии и возможность проведения ленсэктомии. При принятии решения о методике лечения используется ИИ.
Для миопического фенотипа глаукомы характерно медленное прогрессирование, относительно невысокое ВГД. Трудности в постановке диагноза заключаются в определении характера изменений: миопические или глаукомные. По мнению автора, именно применение ИИ повысит эффективность выявления глаукомы в миопических глазах.
Фокально-ишемический фенотип заболевания является генетически обусловленным, проявляется в глаукоме нормального давления (ГНД). Характеристики: фокальный дефект решетчатой мембраны, геморрагии на ДЗН, дефекты хориокапилляров, парацентральные скотомы, медленное прогрессирование, с трудом поддается гипотензивной терапии.
Склеротический фенотип: склероз внутренней сонной артерии, глазной и задних коротких цилиарных артерий нарушает поступление крови к зрительному нерву. В результате не получающая нормального питания решетчатая мембрана трансформируется; при индексе кривизны решетчатой мембраны > 12 прогноз развития заболевания неблагоприятный.
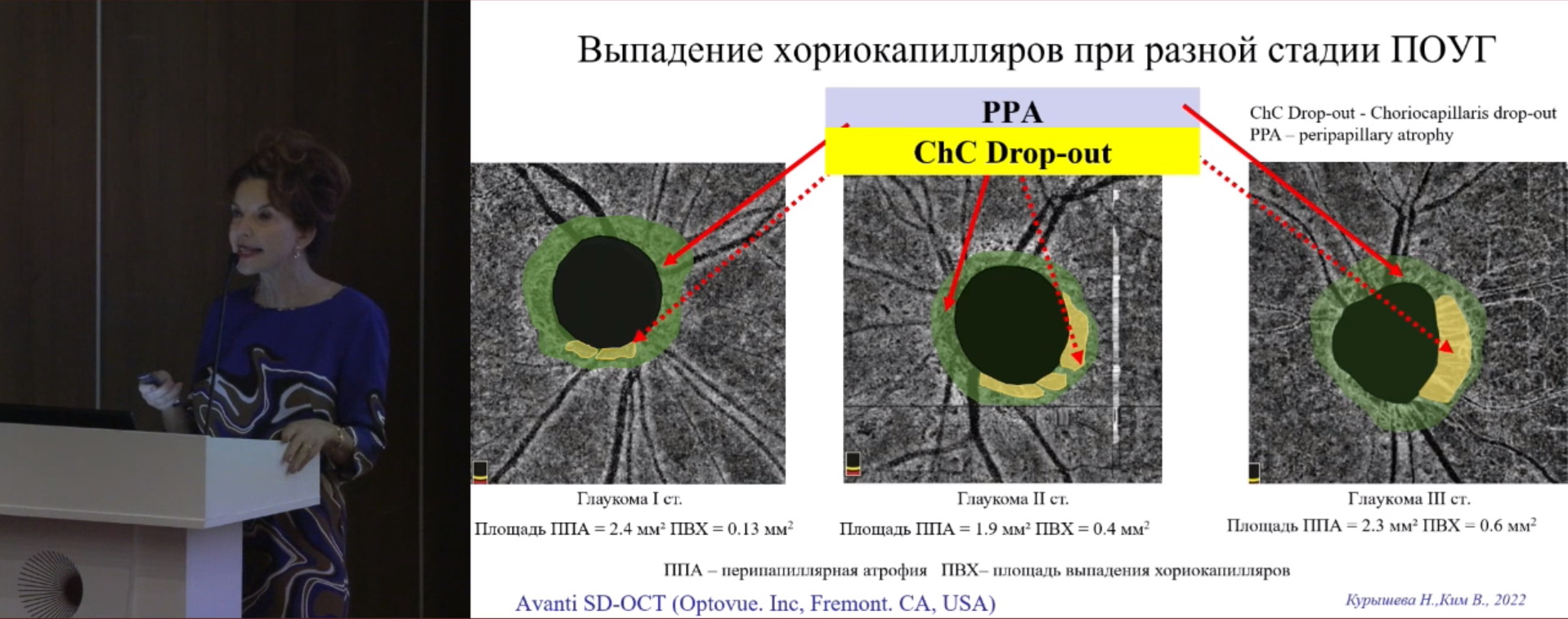
Современные компьютерные томографы высокого разрешения позволяют определять площадь перипапиллярной атрофии (ППА) и площадь выпадения хориокапилляров, увеличивающиеся по мере прогрессирования заболевания (рис. 3).
В заключение профессор Н.И. Курышева подчеркнула, что стартовое лечение глаукомы следует проводить с учетом ее форм и фенотипов, определяемые путем детальной диагностики с применением современных средств визуализации и искусственного интеллекта.
Профессор А.В. Куроедов (Москва) от группы авторов выступил с докладом на тему «Первичная открытоугольная глаукома: основные факторы, способствующие прогрессированию заболевания и определяющие развитие терминальной стадии болезни (по результатам многоцентрового исследования группы «Научный авангард»).
Цель работы заключалась в изучении клинико-демографических характеристик пациента с терминальной стадией ПОУГ и в определении основных предикторов развития этой стадии заболевания.
Задачи: 1. На основе анкетирования изучить спектр мнений врачей-офтальмологов о проблеме терминальной глаукомы (критерии, подходы к диагностике, мониторингу и лечению; 2. Изучить анамнез заболевания от момента постановки диагноза «ПОУГ» до развития ее терминальной стадии; 3. Изучить фенотипические особенности и системные корреляции у пациентов с терминальной стадией ПОУГ; 4. Изучить характер течения заболевания на контрлатеральном глазу у пациентов с имеющейся терминальной ПОУГ на одном глазу.
Дизайн исследования: сбор анамнеза – изучение документации и опрос (в т.ч. отдельные факторы риска, включающие ПЭС, наследственность, системные сосудистые факторы; методы лечения, приверженность к лечению. Методы исследования: общепринятые, дополнительные и специальные офтальмологические методы – визометрия (МКОЗ), тонометрия, рефрактометрия, исследование ПЗО и ЦТР, гониоскопия, стандартная автоматизированная периметрия. В исследовании приняли участие 159 человек (318 глаз) с разными стадиями ПОУГ, при этом на одном глазу – терминальная стадия; второй глаз – контроль. Тип исследования: аналитическое когортное, выборочное, научно-клиническое, многоцентровое.
Возраст пациентов (73 женщины, 96 мужчин) – 72,2 года; продолжительность анамнеза до диагностирования терминальной стадии – 3,9 лет, общий анамнез – 6,3 года; уровень ВГД на момент диагностирования заболевания – 32 мм рт. ст., на момент финального исследования – 23 мм рт. ст.; более 55% пациентов на момент финального исследования получали > 3 антиглаукомных лекарственных препаратов, при этом в контрлатеральный глаз аналогичный объем инстилляций получали 42,8% пациентов; в 74 случаях (46,5%) «терминальный» глаз не был ни разу прооперирован (!).
На рис. 1 можно видеть прогнозирование предсказания терминальной стадии глаукомы.
Наиболее выраженные изменения установлены при сочетании следующих факторов: развитая и далекозашедшая стадии глаукомы на момент установления диагноза; уровень ВГД > 20 мм рт. ст.; выполненная или невыполненная операция в анамнезе; продолжительность анамнеза как ˂ 5 лет, так и > 5 лет. Наименее выраженные изменения установлены при сочетании следующих факторов: начальная стадия глаукомы на момент установления диагноза; уровень ВГД ˂ 20 мм рт. ст. на момент финального исследования; выполненная или невыполненная операция в анамнезе; продолжительность анамнеза как ˂ 5 лет, так и > 5 лет.
Таким образом, ключевое значение имеет своевременность проведения оперативного лечения, а не сам факт его проведения.
Д.м.н. В.П. Николаенко (Санкт-Петербург) сделал доклад «Применение противовоспалительных препаратов в гипотензивной хирургии глаукомы». Как любое повреждение офтальмологические операции индуцируют воспаление, как универсальную защитную реакцию организма, но чрезмерно избыточная воспалительная реакция вследствие многолетнего интенсивного фармакологического воздействия на глазную поверхность пациента с глаукомой чревато утратой фильтрации уже в ранние сроки после синустракулэктомии.
Наряду с антибактериальной, противовоспалительная терапия с одновременным назначением как кортикостероидов, так и НПВС играет ключевую роль в периоперационном сопровождении оперированных по поводу глаукомы пациентов.
«Какую молекулу выгоднее использовать для решения данной задачи?» – задает вопрос докладчик. Всем известный дексаметазон реализует свои многочисленные эффекты через оба известных на сегодняшний день механизма – трансактивации и трансрепрессии, что обуславливает выраженный противовоспалительный, иммуносупрессивный эффект, но и сопутствующую, экспозиционно зависимую офтальмогипертензию. Появившаяся недавно молекула фторметолона реализует свое действие через механизм трансрепрессии, обладает не столь выраженным антифлогистическим эффектом, но его применение не сопровождается риском повышения ВГД. В отличие от слезозаменителей фторметолон существенно снизил популяцию провоспалительных дендритных клеток, не влияя на плотность бокаловидных клеток Бехера, играющих важную роль в поддержании функционирующей фильтрационной подушки. Фторметолон также стимулирует синтез муцинов.
НПВС оказывают влияние на все три фазы воспаления; влияют на конечные этапы метаболизма арахидоновой кислоты, что в практическом отношении означает сопоставимый со стероидами антифлогистический эффект, возможность их одномоментного назначения с ожиданием синергичного эффекта при отсутствии присущих гормонам побочных эффектов. Наиболее подходящей автор назвал молекулу бромфенака с учетом минимальной фармакологической и консервативной нагрузки, обусловленной однократным в течение суток применением.
Предоперационная подготовка. За 1 месяц до планируемой операции следует перевести пациента на БК гипотензивные препараты, что в два раза снижает риск утраты фильтрации; назначение БК слезаменителей; 0,1% фторметолон по 1 капле 4 раза в сутки снижает потребность в манипуляциях с фильтрационной подушкой и возврате к гипотензивным препаратам по сравнению с контролем в 3 раза; при выраженных (уровень 3-4) симптомах и клинических признаках ЗПГ инстилляции 0,09% бромфенака 1 раз в сутки за 2 недели до операции.
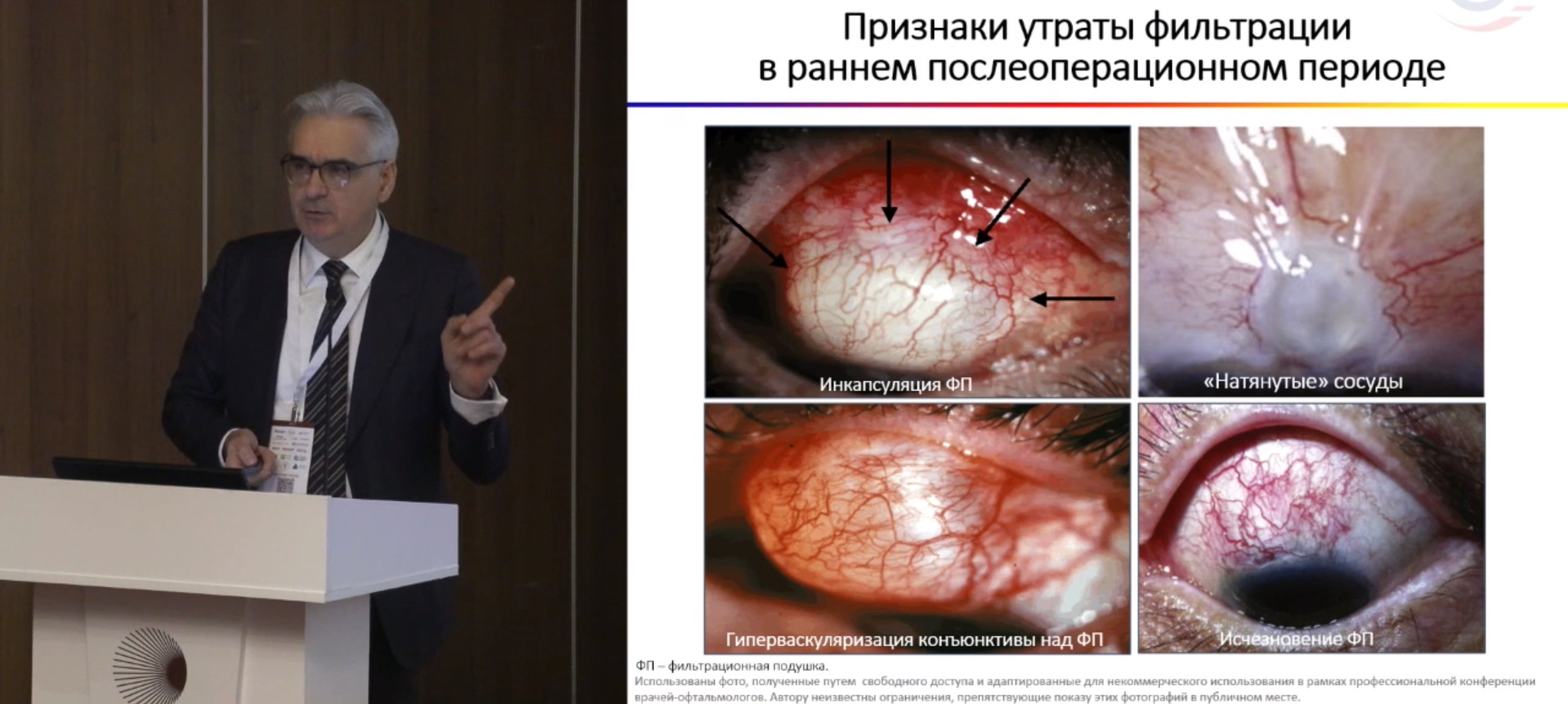
Докладчик обратил внимание на то, что СТЭ обладает выраженным провоспалительным потенциалом, сопоставимым со склеропластической хирургией отслойки сетчатки, что вызывает необходимость применения 0,1% дексаметазона по пролонгированной до 6 недель убывающей схеме с еженедельной отменой одной инстилляции в комбинации с 0,09% бромфенаком в раннем (первые 3 недели) послеоперационном периоде. При часто встречающихся признаках утраты фильтрации в раннем послеоперационном периоде (рис. 1) лечение должно быть пролонгировано до двух и более месяцев с переходом через один месяц с дексаметазона на более безопасный фторметолон с НПВС.
«Профилактика рубцевания в хирургии глаукомы» — тема доклада от группы авторов д.м.н. Е.В. Карловой (Самара). Известно, что успех хирургии глаукомы с годами снижается. Это приводит к поиску путей профилактики рубцевания, в том числе интраоперационной. Применяются антиметаболиты, имеющие тяжелые осложнения, обсуждались возможности применения анти-VEGF препаратов, однако мнения о серьезном повышении эффективности не сложилось.
Эффективной альтернативой являются селективные иммунодепрессанты – циклоспорин А (интраоперационно в дренаже) и эверолимус. В результате проведенных исследований на глазах кроликов были выявлены значительные изменения в морфологии теноновой капсулы, существенное снижение количества фибробластов, высокий уровень профиля безопасности. В настоящее время эверолимус широко и успешно применяется в кардиологии и, по мнению авторов, имеет хорошие перспективы в интраоперационном ведении пациентов с глаукомой, т.к. существует возможность пропитывать этим препаратом дренажные устройства.