Эти факты зафиксированы в последнем Европейском руководстве по диагностике и лечению глаукомы. Следовательно, эти пациенты требуют уже назначения комбинированных лекарственных средств. Речь идет о фиксированных комбинированных формах. Учитывая тот факт, что впервые выявленных больных глаукомой с продвинутыми стадиями глаукомы достаточно много (до 80%), есть все основания начинать гипотензивную терапию у таких пациентов с назначения именно фиксированных комбинированных форм. Преимущества очевидны: удается избегать назначения большого числа препаратов, повышается гипотензивная эффективность, уменьшается число инстилляций, становится более удобным режим, повышается комплаентность и, наконец, экономическая выгода. Кроме эффективного гипотензивного действия, фиксированные комбинации позволяют улучшить приверженность терапии и постоянство в следовании назначениям.
Арсенал фиксированных комбинированных форм достаточен, чтобы сделать правильный выбор (табл. 3).
Компонентами фиксированных комбинаций являются лекарственные средства, относящиеся практически ко всем фармакологическим группам. Но наиболее частые комбинации — это аналоги простагландинов и бета-блокаторы.
В контексте обсуждаемой темы примером может быть Таптиком: комбинация тафлупроста и тимолола малеата (без консерванта).
Комбинация аналогов простагландинов и бета-блокаторов считается наиболее эффективной — это сочетание двух лекарственных средств с различным механизмом действия на гидродинамику глаза. Тафлупрост, как и другие аналоги простагландина, улучшает увеосклеральный отток водянистой влаги в области дренажной зоны и межклеточных пространств ресничного тела. Тимолол — это неселективный бета-блокатор, он блокирует b2-адренорецепторы в эпителии ресничного тела и тем самым угнетает выработку водянистой влаги.
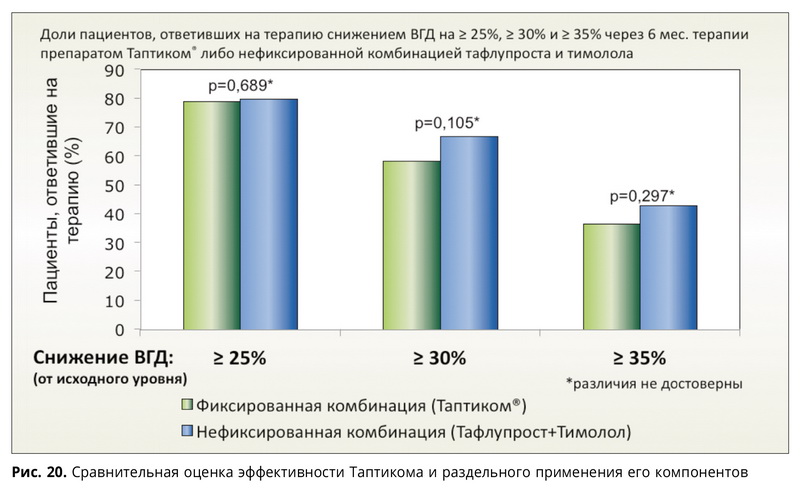
Многочисленные исследования, целью которых было сравнение эффективности, безопасности и переносимости не содержащей консервантов фиксированной комбинации 0,0015% тафлупроста и 0,5% тимолола и нефиксированной комбинации тафлотан+тимолол у пациентов с открытоугольной глаукомой или офтальмогипертензией, показали значительные преимущества фиксированной комбинации (рис. 20).
Снижение ВГД на ≥25% было достигнуто у 79,0% пациентов, получавших фиксированную комбинацию, и у 80,0% пациентов, получавших нефиксированную комбинацию; снижение ВГД на ≥30% — у 58,3 и 66,9% пациентов соответственно; снижение ВГД на ≥35% — у 36,6 и 43,1% пациентов соответственно. Различия между группами не были значимыми (Holló G., Hommer A., Anton A., Ropo A. et al., 2014). Оценка переносимости по 6-балльной шкале свидетельствует о преимуществе Таптикома (рис. 21).
Гиперемия наблюдалась в общей сложности у 8% пациентов в группе фиксированной комбинации и была в основном легко выражена. В отдаленные сроки наблюдения выраженность гиперемии уменьшалась (Holló G., Hommer A., Anton A., Ropo A. et al., 2014). Авторы делают заключение о том, что Таптиком обладает сильным гипотензивным эффектом: снижение ВГД на ≥25% было достигнуто у 79,0% пациентов, получавших фиксированную комбинацию; снижение ВГД на ≥30% — у 58,3% и снижение ВГД на ≥35% — у 36,6% пациентов. Гиперемия была в основном легко выражена и не превышала 8% случаев. Таптиком® не уступает по эффективности, безопасности и переносимости нефиксированной комбинации 0,0015% тафлупроста и 0,5% тимолола.
Перевод на не содержащую консервантов фиксированную комбинацию тафлупрост 0,0015% / тимолол 0,5% (Таптиком) с проводимой ранее монотерапии тимололом или аналогами простагландинов (АПГ) приводил к дополнительному статистически значимому снижению ВГД в каждой из групп (р<0,0001). После перевода пациентов на не содержащую консервантов фиксированную комбинацию тафлупрост 0,0015% / тимолол 0,5% (Таптиком) уменьшились как субъективные симптомы, так и объективные клинические признаки патологии глазной поверхности. Более чем у 80% пациентов перевод на не содержащую консервантов фиксированную комбинацию (Таптиком) с монотерапии тимололом или АПГ приводил к достижению целевого ВГД менее 18 мм рт.ст. Через 4 месяца терапии местная переносимость квалифицировалась как «очень хорошая» или «хорошая» и пациентами, и докторами в 90,1% случаев после перевода с тимолола и в 88,8% случаев при переводе с монотерапии АПГ. В 95% случаев после перевода с тимолола и 90,9% с АПГ пациенты оставались привержены назначенному лечению препаратом Таптиком® и продолжили его после окончания исследования (Pillunat L.E., Ropo A., Kimmich F., 2016).
Заключение
Глаукома часто сочетается с патологией глазной поверхности, в частности с синдромом «сухого» глаза. Многие из доступных в настоящее время препаратов для лечения глаукомы содержат в своем составе консервант бензалкония хлорид — наиболее часто используемый в глазных каплях ингредиент. Его негативное влияние на поверхность глаза было установлено в многочисленных лабораторных (in vitro и in vivo) и клинических исследованиях. Оно включает аллергические и токсические реакции и тем самым увеличивает риск плохой переносимости назначенного лечения. Прежде всего, это вызывает нестабильность слезной пленки, уменьшение количества бокаловидных клеток конъюнктивы, сквамозную метаплазию конъюнктивы, апоптоз, нарушение барьера роговичного эпителия, повреждение глубоких тканей глаза.
Согласно оценкам, не менее 40% пациентов имеют клинические признаки и симптомы раздражения глаз (Jeanen et al., 2007), а многие проявления не обнаруживаются при простом рутинном осмотре. Поэтому важно выслушать больного и провести тщательное исследование его глазной поверхности для выявления любых признаков, указывающих на субклиническую картину воспаления. Сочетание патологии поверхности глаза с применением БХ-содержащих препаратов может оказывать отрицательное влияние и на качество жизни пациентов.
Для пациентов, имеющих высокую чувствительность к консервантам из-за сопутствующей патологии поверхности глаза; получающих комбинированную терапию глаукомы двумя или более препаратами; тем, кому предстоит хирургическое вмешательство по поводу глаукомы, и, наконец, для всех пациентов, нуждающихся в долговременной эффективной и безопасной терапии, антиглаукомные препараты без консерванта обеспечивают клинически значимые преимущества и должны стать золотым стандартом терапии глаукомы в ближайшем будущем.
Литература
- Erb C., Gast U., Schremmer D. German register for glaucoma patients with dry eye. I. Basic outcome with respect to dry eye. Graefe’s Arch Clin Exp Ophthalmol. 2008; 246 (11): 1593–1601.
- Barkman R., Germane M., Karpe G., Malmborg A. -S. Preservatives in eye drops. Acta Ophthalmol. 1969; 47 (3): 461-475.
- Baudoin C., Pisella P.J., Fillacier K. et al. Ocular surface inflammatory changes induced by topical antiglaucoma drugs: human and animal studies. Ophtalmology. 1999; 106: 556-563.
- Leung E.W., Medeiros F.A., Weinreb R.N. Prevalence of ocular surface disease in glaucoma patients. J Glaucoma. 2008; 17 (5): 350–355.
- Wilson W.S., Duncan A.J., Jay J.L. Effect of benzalkonium chloride on the stability of the precorneal tear film in rabbit and man. Br J Ophthalmol. 1975; 59: 667-669.
- Schwab I.R., Linberg J.V., Giola V.M. et al. Foreshortening of the inferior conjunctival fornix associated with chronic glaucoma medications. Ophtal-mology. 1992; 99: 197-202.
- De Saint Jean M., Brignole F., Bringuier A.F., Bauchet A., Feldmann G., Baudouin C. Effects of benzalkonium chloride on growth and survival of Chang conjunctival cells. Invest Ophthalmol Vis Sci. 1999; 40: 619-630.
- De Saint Jean M., Debbasch C., Brignole F., Rat P., Warnet J.M., Bau-douin C. Toxicity of preserved and unpre-served antiglaucoma topical drugs in an in vitro model of conjunctival cells. Curr Eye Res. 2000; 20: 85-94.
- Pisella P.J. Conjunctival markers as predictable markers for preoperative glaucoma assessment. Br J Ophthalmol. 2006; 90 (11): 1335—1336.
- Pisella P.J., Debbasch C., Hamard P., Creuzot-Garcher C., Rat P., Brignole F., Baudouin C. Conjunctival proinflammatory and proapoptotic effects of latanoprost and preserved and unpreserved timolol: an ex vivo and in vitro study. Invest Ophthalmol Vis Sci. 2004; 45: 1360—1368.
- Pisella P.J., Fillacier K., Elena P.P., Debbasch C., Baudouin C. Comparison of the effects of preserved and unpreserved formulations of timolol on the ocular surface of albino rabbits. Ophthalmic Res. 2000; 32: 33–38.
- Pisella P.J., Pouliquen P., Bau-douin C. Prevalence of ocular symptoms and signs with preserved and preservative free glaucoma medication. Br J Oph-thalmol. 2002; 86 (4): 418-423.
- Ariturk N., Oge I., Baris S., Erkan D., Koc F. The effects of antiglaucomatous agents on conjunctiva used for various durations. Int Ophthalmol. 1996–1997; 20 (1–3): 57–62.
- Авдеев Р.В., Александров А.С., Басинский А.С., Блюм Е.А., Брежнев А.Ю. и др. Клиническое многоцентровое исследование эффективности синусотрабекулэктомии. Национальный журнал глаукома. 2013; 12 (2): 53–60.
- Еричев В.П., Амбарцумян К.Г., Федоров А.А. Клинико-морфологические доказательства влияния консервантов на поверхность глаза при первичной открытоугольной глаукоме. Национальный журнал глаукома. 2014; 13 (4): 13-22.
- Онищенко А.Л., Лихачева И.Г., Пластинина С.Л., Ткачев В.А. Причины низкой комплаентности больных глаукомой и пути ее коррекции. Глаукома. 2009; 4: 39–42.
- Chung S.H., Lee S.K., Cristol S.M., Lee E.S., Lee D.W., Seo K.Y., Kim E.K.
Impact of short-term exposure of commercial eyedrops preserved with ben-zalkonium chloride on precorneal mucin. Mol Vis. 2006; 12: 415-421.
- Codling C.E., Hann A.C., Mail-lard J.Y., Russell A.D. An investigation into the antimicrobial mechanisms of action of two contact lens biocides using electron microscopy. Cont Lens Anterior Eye. 2005; 28: 163-168.
- Codling C.E., Jones B.V., Mahen-thiralingam E. et al. Identification of genes involved in the susceptibility of Serratia marcescens to polyquate-rnium-1. J Antimicrob Chemother. 2004; 54: 370-375.
- Becquet F., Goldschild M., Moldovan M.S., Ettaiche M., Gastaud P., Baudouin C. Histopathological effects of topical ophthalmic preservatives on rat corneoconjunctival surface. Curr Eye Res. 1998; 17 (4): 419–425.
- Lin P.Y., Cheng C.E. et al. Pre-valence of dry eye among an elderly chinese population in Taiwan: the shihpai eye study. Ophthalmology. 2003; 110: 1096–1101.
- Uusitalo H. et al. Acta Ophthal-mol. 2010; 88: 329-336.
- Egorov E., Ropo A. et al. Eur J Ophthalmol. 2009; 19 (2): 214-222.
- Pfeiffer N., Traverso C.E., Lorenz K., Saarela V., Liinamaa J., Uusitalo H., Astakhov Y., Boiko E., Ropo A. A 6-month study comparing efficacy, safety, and tolerability of the preservative-free fixed combination of tafluprost 0.0015% and timolol 0.5% versus each of its individual preservative-free components. Adv Ther. 2014; 31 (12): 1228—1246.
- Holló G., Hommer A., Anton A., Ropo A. et al. Efficacy, safety, and to-lerability of preservative-free fixed com-bination of tafluprost 0.0015%/timolol 0.5% versus concomitant use of the ingredients. J Ocul Pharmacol Ther. 2014; 30 (6): 468-475.
- Pillunat E., Ropo A., Kimmich F. Результаты мультицентрового, неинтервенционного исследования пациентов с глаукомой и офтальмогипертензией бесконсервантной фиксированной комбинацией тафлупрост 0,0015% / тимолол 0,5%. В кн.: EGS Congress: Сб. тез. Prague, 2016; June 19-22.
- Pfeiffer N.N., Pillunat L.E., Ropo A. Оценка эффективности, переносимости и безопасности не содержащей консервантов фиксированной комбинации тафлупроста 0,0015%/тимолол 0,5% у пациентов, ранее получавших монотерапию препаратами аналогами простагландина или тимолола. В кн.: EGS Congress: Сб. тез. Prague, 2016; June 19-22.