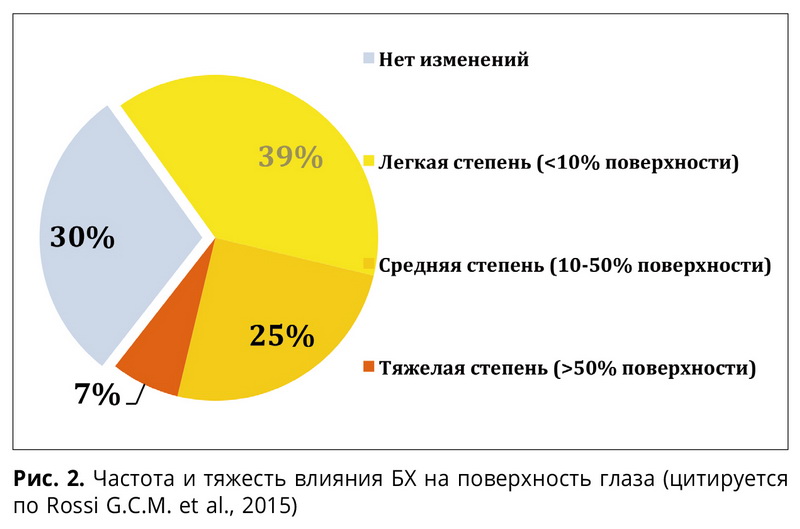
Как показывают многочисленные исследования, БХ не безразличен для тканей поверхности глаза. Он почти в 70% случаев вызывает на глазной поверхности изменения той или иной степени выраженности (рис. 2).
Экспериментальными исследованиями доказан дозо- и времязависимый эффект токсических проявления БХ на эпителиальные клетки тканей поверхности глаза (табл. 2).
Многочисленные экспериментальные исследования лишь подтверждают токсический эффект БХ. Работы C. Xiong et al. (2008) свидетельствуют о том, что 0,1% БХ вызывает патологические изменения поверхности глаза кроликов, совпадающие с ССГ у человека, и это выражается в снижении базальной секреции, уменьшении плотности бокаловидных клеток, снижении секреции муцина (недостаточность MUCSAC).
Негативные эффекты БХ складываются из трех основных действий, приводящих к появлению субъективных и объективных признаков ССГ: БХ обладает свойствами детергента, вступающего в реакцию с липидами слезной пленки; непосредственно повреждает эпителий роговицы и конъюнктивы; вызывает иммуноаллергические реакции.
Исследования позволили понять последовательность токсического действия БХ (рис. 3). Первым и очень важным звеном в этой цепи патологических изменений является нарушение стабильности прероговичной слезной пленки, и, если воздействие агента продолжается (а при глаукоме именно так и происходит), процесс завершается выраженным токсико-аллергическим воспалением и апоптозом.
БХ в глазных растворах многоразового применения обычно используют в концентрации 0,01% (от 0,004 до 0,02%). По статистике, 84% глаукомных больных используют глазные капли с консервантами (БХ+), 13% — без консервантов (БХ–) и 3% — комбинацию капель (БХ+ и БХ–). Субъективные признаки ССГ (жжение, ощущение инородного тела, сухость, зуд) при использовании капель, содержащих БХ, встречаются более чем в 2 раза чаще, а при переводе больных на капли без БХ состояние поверхности глаза значительно улучшается.
Очень важным является влияние БХ на слезную пленку (СП). СП выполняет важную функцию защиты, увлажнения и обеспечивает трофику роговицы, а ее гомеостаз поддерживается гормональными и нейрональными механизмами. Кроме этого, слезная пленка выполняет светопреломляющую и светопроводную функции. Любые нарушения регуляции или изменения в составе СП (особенно при изменении гормонального фона организма) могут привести к запуску механизмов, приводящих к каскаду нарушений функции слезопродукции, к воспалительным реакциям, а в дальнейшем — к деструкции добавочных слезных желез и эпителия конъюнктивы.
СП имеет трехслойную структуру, устойчивость и непрерывность которой между мигательными движениями является ее важнейшими характеристиками и определяют ее функциональное состояние. Наружный, липидный слой вырабатывается мейбомиевыми железами век и железами Цейса и представлен полярными и неполярными липидами. Роль этого слоя огромна: являясь барьером между внешней средой и глазом, он снижает поверхностное натяжение слезной жидкости, замедляет испарение воды с глазной поверхности на 90–95%, осуществляет защитную функцию, регулирует процесс теплоотдачи.
БХ, обладая свойством детергента, усиливает эвапорацию (испарение) и вызывает нестабильность СП. Этот эффект был описан в 1985 году, а в дальнейшем нашел дополнительные подтверждения. На здоровых добровольцах было показано значительное укорочение неинвазивного времени разрыва слезной пленки (ВРСП) через 30 мин после инстилляции тимолола, содержащего БХ, в то время как тимолол без консерванта не имел такого эффекта. Под влиянием обеих форм тимолола (в бóльшей степени БХ+ тимолола) становилась положительной флюоресцеиновая проба.
При вторичном ССГ меняется качественный и количественный состав СП. Для количественного измерения слезопродукции применяют тест Ширмера 1, предложенный еще в 1903 году и определяющий суммарную (базальную и рефлекторную) слезопродукцию. Но в связи с выявленной плохой повторяемостью данных классического теста Ширмера 1 без анестезии, предложен вариант с предварительной инстилляционной анестезией, на результаты которого практически не влияет раздражение глазной поверхности тест-полоской. Этот тест получил название теста Ширмера 2 с анестезией (в отечественной литературе его чаще называют пробой Джонса, или тестом на базальную секрецию).
Влияние БХ на основную слезопродукцию является незамедлительным, но обратимым, так как длительные инстилляции не вызывают прогрессивно уменьшающуюся со временем слезопродукцию. Перевод больных на капли без консервантов приводит к нормализации слезопродукции уже через 2 недели даже у тех больных, которые годами получали БХ-содержащие капли. Но консерванту присущи не только это непосредственное влияние, но и те, которые длительное время не имеют яркой манифестации, поэтому могут быть упущены и вовремя не выявлены. К одному из этих опосредованных воздействий относят снижение плотности бокаловидных клеток конъюнктивы, являющихся наиболее важным показателем, отражающим состояние муцинового слоя и глазной поверхности в целом.
Другие многочисленные экспериментальные исследования лишь подтверждают токсический эффект БХ. Работы C. Xiong et al. (2008) свидетельствуют о том, что 0,1% БХ вызывает патологические изменения тканей поверхности глаза кроликов, совпадающие с клинической картиной ССГ у человека, и это выражается в снижении базальной секреции, уменьшении плотности бокаловидных клеток, снижении секреции муцина (недостаточность MUCSAC).
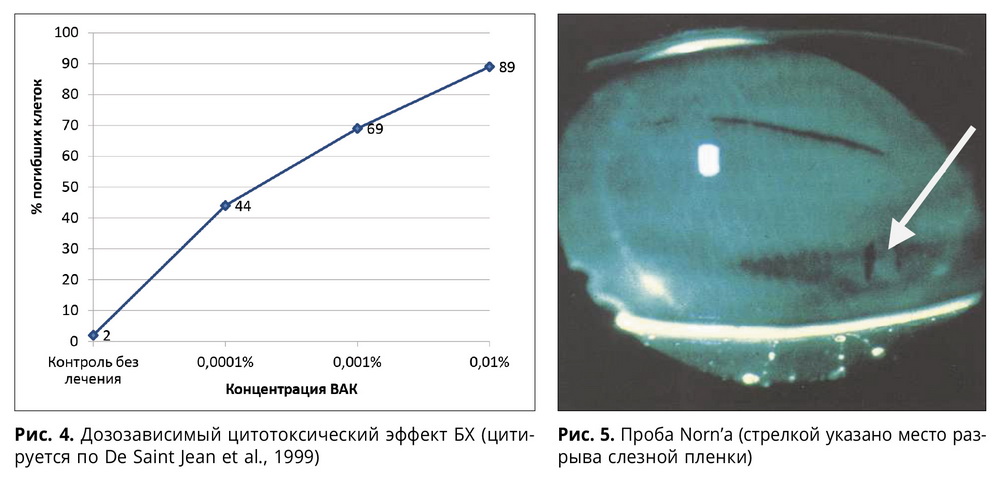
Более того, De Saint Jean et al. (1999) выполнили исследование с целью изучения специфических воздействий БХ на клетках эпителия конъюнктивы in vitro. Линию клеток конъюнктивы человека (производное Wong-Kilbourne от конъюнктивы Chang) подвергали воздействию БХ в концентрациях от 0,01 до 0,0001% с экспозицией в 10 минут. Оценивали апоптоз, число и жизнеспособность клеток, морфологию клеточного ядра и цитоскелета. При этом было показано, что даже при самой низкой концентрации (0,0001%) БХ приводил к гибели 44% культуры клеток конъюнктивы (рис. 4).
Сравнивали токсичность 0,005% латанопроста, 0,5% тимолола (в обоих случаях в качестве консерванта был 0,02% БХ), 0,5% тимолола без консерванта и отдельно 0,02% БХ при их воздействии на линию клеток конъюнктивы человека (Wong–Kilbourne) (Pisella P.J. et al., 2004). В качестве контроля использовали клетки, на которые воздействия не было. Исследование проводили по специальному протоколу. Жизнеспособность клеток оценивали с использованием цитофлуорометрии с нейтральным красным и конденсации хроматина по тесту Hoechst 33342. Изменения цитоскелета оценивали при помощи конфокальной микроскопии. Данные, указывающие на то, что оба препарата были менее токсичны, чем БХ сам по себе, являются в определенной степени интригующими и свидетельствуют о том, что сам консервант оказывает, возможно, бóльший отрицательный эффект, чем консервант в составе лекарственного средства.
Нежелательные эффекты БХ складываются из трех основных действий, приводящих к появлению субъективных и объективных признаков ССГ. Они хорошо известны: он обладает свойствами детергента, вступающего в реакцию с липидами слезной пленки; непосредственно повреждает эпителий роговицы и конъюнктивы; вызывает иммуноаллергические реакции.
Мы уже говорили о том, что у больных ПОУГ, длительно получавших гипотензивное лечение, выявили значительное снижение базальной секреции (тест Ширмера) и времени разрыва слезной пленки (недостаточность водного и липидного компонентов) по сравнению с данными контрольной группы, а проведенная импрессионная цитология показала статистически значимое снижение плотности бокаловидных клеток, что проявлялось вторичной недостаточностью муцинового слоя.
Характерны и клинические проявления в результате постоянного механического раздражения век и хронического воспаления при ССГ. Чаще всего они характеризуются следующим: при биомикроскопии хорошо видны параллельные нижнему веку складки конъюнктивы, что приводит к жалобам на ощущение инородного тела, а их постоянное травмирование во время моргания может явиться причиной рецидивирующих субконъюнктивальных кровоизлияний; появление конъюнктивального отделяемого, слизистых (эпителиальных) нитей; медленное «отлипание» тарзальной и бульбарной конъюнктивы при оттягивании нижнего века или при попытке поднять верхнее веко. Такой признак, как появление нитей на роговице, следует связывать с прогрессированием роговичного ксероза. Субъективные признаки, в свою очередь, можно разделить на специфические и параспецифические. К первым можно отнести болевую реакцию на инстилляции индифферентных глазных капель; плохую переносимость ветра, холодного и кондиционированного воздуха, дыма и т.д.; ощущение «сухости» в глазу. Длительное пребывание в таких условиях может сопровождаться разной степени выраженности дискомфортом и другими субъективными ощущениями. Но все-таки наиболее частой жалобой остается слезотечение, которое в начальных стадиях ССГ можно рассматривать как компенсаторный механизм.
С практической точки зрения наибольшее клиническое значение приобрели методы исследования прероговичной слезной пленки и слезопродукции.
Для этой цели используют пробу Norn’а (рис. 5). Пациенту в конъюнктивальную полость инстиллируют одну каплю 0,1-0,2% раствора флюоресцеина натрия. Включают готовую к работе щелевую лампу. Пациента просят сделать одно мигательное движение и смотреть прямо перед собой с широко открытой глазной щелью, не мигая. На этом этапе врач включает секундомер и наблюдает за окрашенной флюо-ресцеином поверхностью роговицы, постоянно перемещая микроскоп и контролируя всю эпителиальную поверхность до появления разрыва в слезной пленке. Разрыв представляется в виде темной неровной, иногда с ответвлениями полоски или пятна неправильной формы. Время от последнего мигательного движения до появления разрыва называют временем разрыва слезной пленки (ВРСП).
ВРСП у здоровых в возрасте до 35-40 лет составляет в среднем 20 сек. С возрастом это время уменьшается и к 70-80 годам составляет около 11-12 сек. При ВРСП менее 10 сек можно говорить о нестабильности прероговичной слезной пленки.