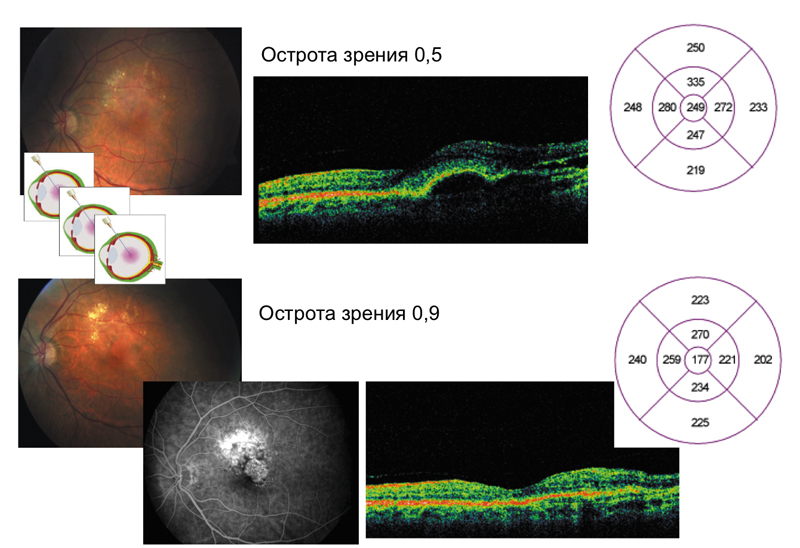
Возникает другой вопрос: «Сколько инъекций необходимо проводить?» Приведу еще один клинический случай (слайд 11):
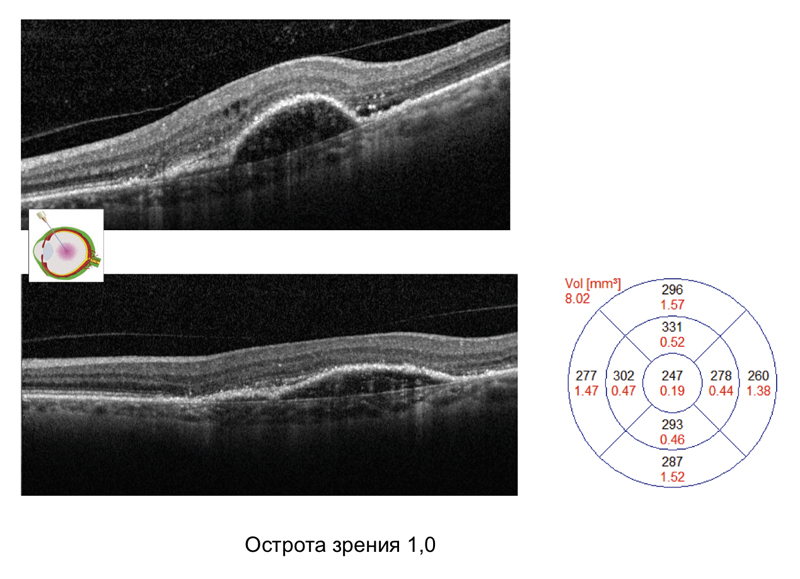
мы провели пациентке 3 инъекции, острота постепенно приблизилась к 0,9, в макулярной зоне все «лежит», и на первый взгляд, стоит остановиться. Проводим флюоресцентную ангиографию, видим, что часть мембраны, которая ближе к макуле «запустела», но та часть мембраны, которая лежит выше, достаточно активна — провели еще одну инъекцию. На слайде 12 представлен срез в зоне бывшей наибольшей активности, где видно, что активности нет, острота — 1,0, пациентка находится под наблюдением.
Другой клинический случай: массивная мембрана, проведено 3 инъекции, острота зрения повысилась, отек уменьшился, но при ангиографии мы видим активность мембраны. Пациентке была предложена инъекция (это было в мае), но пациентка предпочла дачу. Через два месяца зрение упало до сотых долей, и, несмотря на дальнейшие ИВВ, острота зрения выше 0,02 не поднялась. Этот пример дает ясно понять, насколько велико значение временного фактора.
Таким образом, после анализа различных рандомизированных исследований было показано, что только ¼ пациентов достигает стабильности после 3-х инъекций. ¾ пациентов из-за позднего обращения за лечением не достигают желаемой стабильности. Что такое критерий стабильности остроты зрения? Когда разница между максимальной и минимальной остротой зрения между приемами не превышает трех букв по EDTRS или находится в пределах одной строчки по Сивцеву-Головину, можно говорить о стабильности зрения.
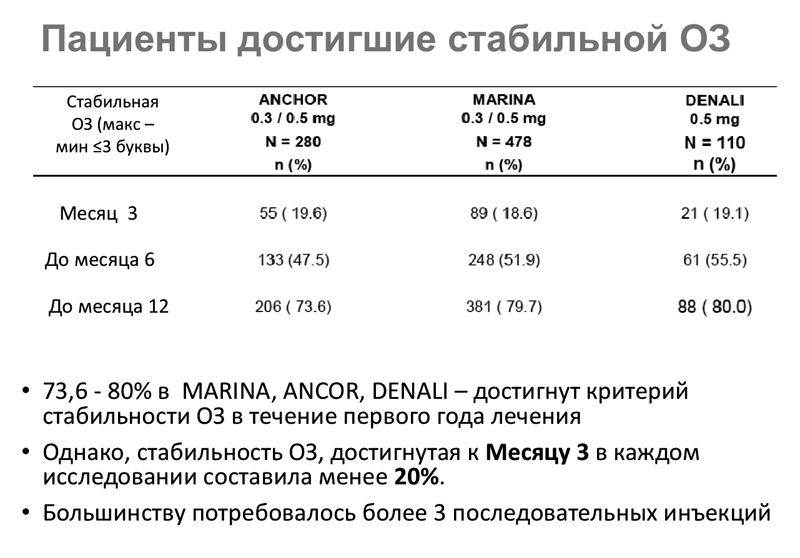
На слайде 13 представлены результаты трех исследований: ANCHOR, MARINA, DENALE, при которых люцентис вводился ежемесячно. Если мы проанализируем 3-й месяц, увидим, что только 20% пациентов достигли стабильной остроты зрения, к 12-му месяцу эта цифра значительно выросла. Следовательно, мы должны продолжать ИВВ луцентиса до достижения стабильной максимальной остроты зрения, которое должно быть диагностировано на трех последующих месячных визитах. Пока мембрана «открыта», ни о каком медицинском спокойствии речи быть не может.
Что дальше? На сегодняшний день сайт clinicaltrials.gov (Национального института здоровья США) содержит результаты более 1000 зарегистрированных клинических исследований, из них к VEGF относятся всего 199 исследований, к новым видам препаратов — 952 исследования. Какие требования в настоящее время предъявляются к новым препаратам, которые будут применяться в лечении экссудативной формы возрастной макулярной дегенерации? Прежде всего, лечение должно быть патогенетическим, должен быть синергизм действия, который должен приводить к индукции не только запустевания роста новообразованных сосудов, но и предотвращению их нового появления.
В настоящее время во многих исследовательских центрах ведется большое количество исследований по новым препаратам, уже завершены большинство IIА стадий клинических исследований. Одной из интересных «новинок» являются ингибиторы интегриновых рецепторов ALG-1001 фирмы Allegro Ophthalmics. Если анти-VEGF терапия убирает кровоизлияния и отек посредством запустевания новообразованных сосудов, ингибирование интегринов дополнительно препятствует появлению новых зон роста, т.е. это более эффективный препарат. Но препарат оказался очень «дозозависимым»: 2 мг и стрелка идет вниз, т.е. никакой эффективности; 2,3 мг — мы выходим на плато (стабильная острота зрения); 3,2 мг — заметное улучшение зрения у пациентов с экссудативной формой ВМД.
Следующий препарат — Fоvista (E10030; anti-PDGF-B). Его действие направлено на ингибирование фактора роста тромбоцитов. Как известно, неоваскулярная мембрана меняет свою форму и клеточный состав на протяжении всей своей жизни. Это можно сравнить с ростом дерева — дерево растет: почка — молодые побеги — формирование плотной коры — появление большого количества листьев. Так и здесь: сначала «идут» эндотелиальные клетки, вслед за ними — перициты, затем — фибробласты. В некоторых случаях, когда после анти-VEGF терапии мы делаем ангиографию, иногда видим подобие дерева: экссудации нет, но «дерево» видим. Это «дерево» с большим количеством перицитов. Ингибирование факторов роста эндотелия сосудов на это «дерево» никак не действует. В данном случае и будет «работать» препарат Fоvista, который действует на перициты. В клинических исследованиях его применяют совместно с анти-VEGF терапией, т.к. ингибирование VEGF действует на эндотелий, а ингибирование фактора роста пигментного эпителия действует на перициты.
Моноклональные антитела к сфин-гозин-1-фосфату (Sonepcizumab). К сожалению, пока этот препарат прошел только первую стадию клинических исследований, на которой была доказана его безопасность для эндовитреального введения. В основе действия сфингозина лежит интеграция всех цитокинов, в т.ч. фактор роста эндотелия сосудов и интегринов, т.е. это как регулирующий белок. И когда мы ингибируем этот регулирующий белок, мы предотвращаем рост новообразованных сосудов. Другими словами, этот препарат рассчитан на пациентов, которые стоят на пороге развития неоваскуляризации.
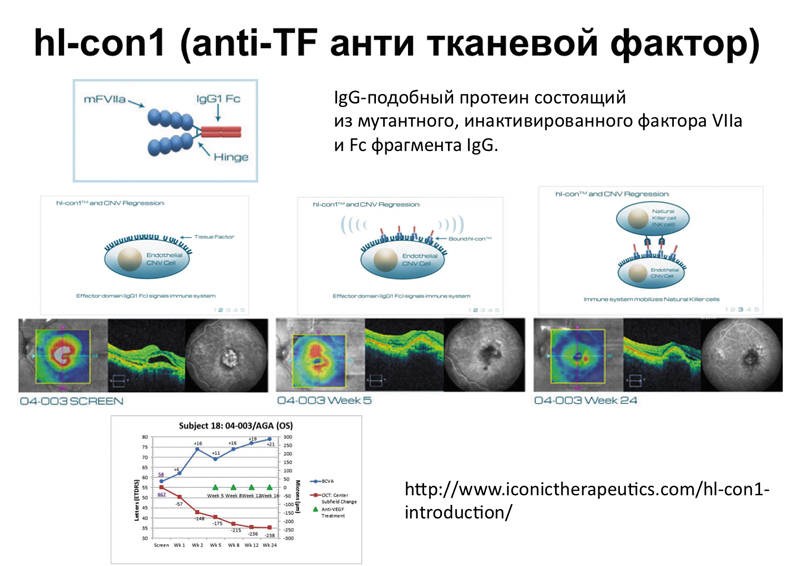
Самый интересный по механизму действия — антитканевой фактор, IgG-подобный протеин, состоящий из мутантного, инактивированного фактора VIIа и Fc фрагмента IgG. Препарат очень интересно устроен: одним концом он крепится к эндотелиоциту, другим концом вызывает адгезию натуральных киллеров, т.е. организм сам убивает клетки новообразованных сосудов. На сегодняшний день завершена IIА стадия клинических исследований. На слайде 14 видно, насколько хорошо запустевает ложе новообразованных сосудов, насколько хорошо повышается острота зрения вследствие уменьшения отека нейроэпителия.
Таким образом, сегодня мы живем в эру интравитреальных инъекций, мы ждем появления новых препаратов, не забываем о профилактике, не забываем о том, что чем раньше мы начинаем делать ИВВ анти-VEGF препаратов пациентам с уже имеющейся субретинальной неоваскулярной мембраной, тем больше шансов вернуть им зрение.