Роль ингибиторов ангиогенеза в антиглаукомной фильтрационной хирургии. Как уже указывалось выше, эффективность и безопасность антиглаукомной фильтрационной хирургии зависит от того, на каком фоне она выполняется. Если рубеоз УПК и радужки не подвергся обратному развитию к моменту выполнения операции, хирургия глаукомы чревата большим количеством осложнений и, скорее всего, окажется неэффективной. Поэтому, если панретинальная коагуляция не привела к регрессу неоваскуляризации в переднем отрезке глаза или если она не могла быть выполнена из-за низкой прозрачности оптических сред глаза, оправдано первоначальное проведение интравитреального введения бевацизумаба, и только после регресса новообразованных сосудов, наступающего обычно уже в ближайшие дни после инъекции, необходимо проводить фильтрационную хирургию.
J.B. Jonas с соавт. [80] описали 2 пациентов, которым была выполнена стандартная противоглаукомная проникающая фильтрационная хирургия в сочетании с интравитреальным введением бевацизумаба. У обоих пациентов внутриглазное давление составляло 10-14 мм рт.ст. в течение 12 недель после операции. Авторы сделали вывод о том, что инъекция бевацизумаба может оказаться хорошим вспомогательным средством при проведении фильтрующих операций при неоваскулярной глаукоме.
Исследования T.M. Eid с соавт. [81] показали, что использование дренажа Ахмеда в сочетании с предварительной инъекцией бевацизумаба значительно уменьшает частоту хирургических осложнений. По их данным, риск операционных и послеоперационных осложнений оказался выше на глазах с упорной неоваскуляризацией радужки, рефрактерной к панретинальной лазеркоагуляции. Наилучший успех дренажной хирургии (85%) был достигнут у пациентов, которым первоначально выполнили ПРК и интравитреальную инъекцию бевацизумаба. Если требуемый объем панретинальной лазеркоагуляции не был выполнен до имплантации дренажа, его необходимо дополнить в кратчайшие сроки после хирургической операции, что значимо улучшает частоту успешной дренажной хирургии и уменьшает потребность в повторных интравитреальных инъекциях бевацизумаба.
Необходимо помнить, что ключом к безопасной и успешной дренажной хирургии является регресс рубеоза радужки и угла передней камеры после корректно выполненной панретинальной лазеркоагуляции в целях устранения ишемии сетчатки. У пациентов со значительным повышением ВГД, «цветущей» неоваскуляризацией радужки и непрозрачными оптическими средами глаза (отек роговицы, катаракта, витреальная геморрагия и т.п.) выполнение адекватной ПРК невозможно. В таких случаях предпринятая глаукомная операция таит в себе высокий риск осложнений и, как правило, неэффективна.
В подобных ситуациях комбинированная хирургия, включающая использование ингибиторов ангиогенеза и дренажей, может стать весьма перспективным направлением [81].
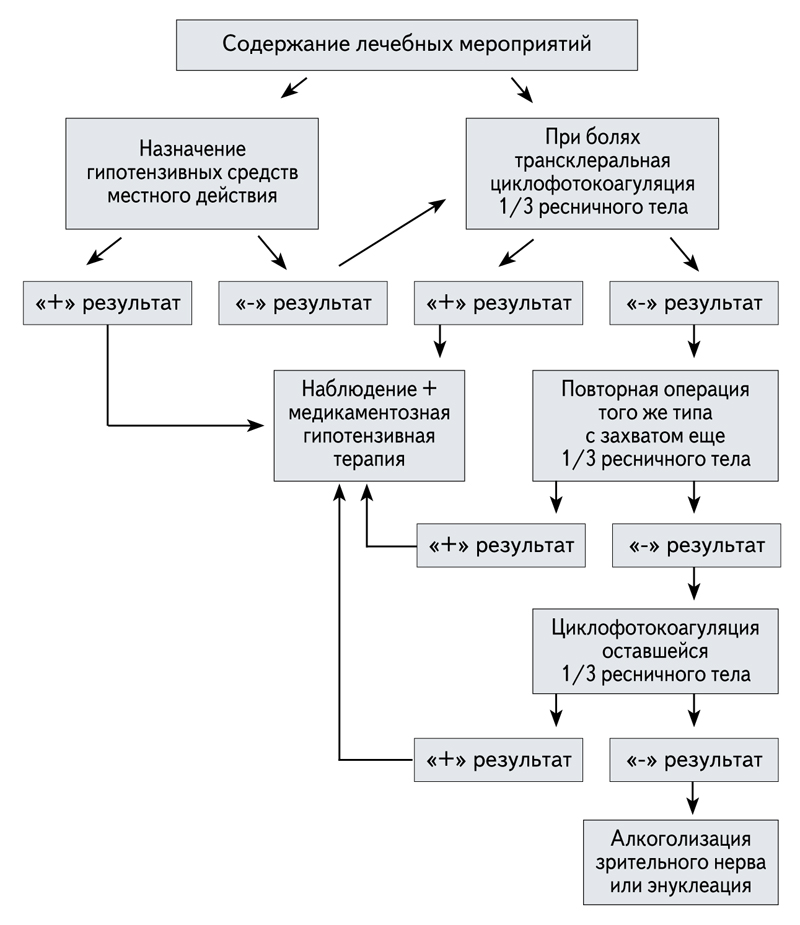
Если «полезное зрение» у пациента отсутствует, то незамедлительно должна быть назначена медикаментозная гипотензивная терапия. Последующая тактика курации пациента определяется в зависимости от того, есть ли у пациента боли в глазу и какова степень их выраженности (алгоритм 4).
Методом выбора в подобных клинических ситуациях являются процедуры, приводящие к разрушению части цилиарного тела. Наиболее часто применяемой в настоящее время является диодная лазерная трансклеральная циклокоагуляция.
В 1972 году H. Beckman и J. Waeltermann [82] выполнили первую транссклеральную циклофотокоагуляцию с использованием рубинового лазера. В последующем для этой цели были использованы Nd:YAG с удвоением частоты и диодные лазеры.
Трансконъюнктивальная циклокоагуляция является асептической процедурой и в большинстве случаев производится амбулаторно. Методика вмешательства состоит в следующем [83, 84]. После инстилляционной анестезии ретробульбарно вводят 2 мл 2% раствора новокаина или лидокаина, иногда из двух точек, расположенных у наружной и внутренней спаек нижнего века. Через 15 минут после инъекций на расстоянии 1,5 мм от лимба и концентрично ему наносят 15-20 аппликаций при перпендикулярном расположении наконечника зонда и легком давлении им на склеру. Мощность и экспозиция лучевого воздействия определяются типом лазера и составляет для диодного коагулятора (λ=810 nm) 0,5-1,0 Вт и 0,5-2,0 с, соответственно, а для неодимового лазера (λ=1060 nm) — 4-6 Вт и 1,0-5,0 с, соответственно. При этом адекватная степень воздействия достигается за счет постепенного повышения дозы излучения до момента, когда конъюнктива в зоне вмешательства побледнеет. Рубцевание ресничных отростков цилиарного тела завершается через 2-3 недели [85]. В первые три недели после операции у больных, как правило, развивается иридоциклит, нередко с реактивной гипертензией, и могут обостриться боли, что требует назначения анальгетиков, нестероидных противовоспалительных средств, кортикостероидов, ингибиторов карбоангидразы (диакарб в день операции и в первые сутки после нее), а также продолжения местной медикаментозной гипотензивной терапии, но без применения простагландинов [86]. При недостаточном гипотензивном эффекте операцию можно повторять 2-3 раза с интервалом в 1 месяц и более [84].
По данным А.Б. Качанова [83], уже через сутки после операции у 98% больных отмечался существенный анальгетический эффект, а через 2 суток снижение офтальмотонуса наблюдалось у 88,2% пациентов, сохранявшееся в течение года у 43,3% больных. При этом через 18 месяцев после операции у части больных наблюдалось обратное развитие рубеоза радужки.
По мнению A. Oguri с соавт. [87], излучение диодного лазера более эффективно, чем непрерывная волна Nd:YAG лазера. Данный вывод сделан на основании того, что в 10% случаев после Nd:YAG-лазерной деструкции развилась субатрофия глазного яблока, в то время как после диодной циклокоагуляции этого не наблюдалось ни разу. В исследовании P.A. Bloom с соавт. [88] получили уменьшение ВГД на 53% при среднем уровне предоперационного ВГД в 45 мм рт.ст.
Несмотря на хороший гипотензивный эффект циклофотокоагуляции, процент больных, теряющих зрение после данной операции, по данным M.B. Shields и S.E. Shields [89], остается достаточно большим и составляет 46,6%, поэтому в настоящее время данную технологию не рекомендуют использовать на глазах, которые еще имеют «полезное зрение».
Криотерапия цилиарного тела, впервые описаная G. Bietti в 1950 году [90] и обладающая хорошим гипотензивным эффектом, в настоящее время уже не используется в связи с высоким риском послеоперационных осложнений: развитие субатрофии глазного яблока, симпатической офтальмии, отслойки сетчатки, ишемии переднего сегмента и др. [91]. Кроме того, в исходе лечения до 70% пациентов с НВГ после криоциклотерапии теряют зрение [92].
Попытки хирургического удаления части цилиарного тела также привели к снижению внутриглазного давления. Однако, исходя из данных ретроспективного анализа 90 подобных случаев, сделанного в 1984 году H. Sautter и U. Demeler [93], на 13 глазах отмечались серьезные интраоперационные осложнения, в том числе интравитреальные кровоизлияния (4 глаза), выпадение стекловидного тела (8 глаз), и экспульсивная гемморагия (1 глаз). Через 6 месяцев на 4 глазах развилась гипотония, причем на одном глазу с формированием субатрофии глазного яблока. Еще в одном глазу диагностирована отслойка сетчатки. При этом ВГД было менее 19 мм рт.ст. на 60 глазах через 6 месяцев после операции. В настоящее время из-за риска осложнений эта процедура уже не используется.
Далее, если пациент не испытывает болей в глазу, необходимо ограничиться только наблюдением. При отсутствии анальгезирующего эффекта от циклодеструкции и гипотензивной медикаментозной терапии возможна алкоголизация зрительного нерва. И только в крайнем случае, при сохранении нестерпимых болей в глазу, можно предложить больному энуклеацию больного глаза.
Несмотря на определенные успехи в лечении больных с неоваскулярной глаукомой, прогноз в отношении длительной сохранности у них высокой остроты зрения остается все еще плохим. Ключ к достижению более впечатляющих результатов лежит в реально раннем выявлении у всех диабетиков неоваскуляризации в области угла передней камеры и радужки и своевременном лечении развивающейся ретинопатии, то есть в проведении адекватной панретинальной лазеркоагуляции.