Современные методы лечения БСП
Несмотря на успехи в изучении этиологии и патогенеза БСП, лечение этих больных представляет собой весьма сложную и все еще далекую от оптимального решения задачу. Терапия БСП имеет этиологическую и симптоматическую направленность в зависимости от причины возникновения основного заболевания. Однако исследований в этой области пока недостаточно. Вместе с тем имеются отдельные сообщения, указывающие на особенности лечения в зависимости от этиологии БСП. Пациентам с синдромальными проявлениями показано проведение базовой терапии и наблюдение у специалистов соответствующего профиля. При условии наличия ограниченной офтальмологической симптоматики проводится местное лечение.
Необходимо уже на ранних стадиях назначать нефармакологическое лечение, которое включает информирование пациента о причинах заболевания, о необходимости проведения гигиены век и согревающих процедур, массажа, физиотерапии и т.д., о факторах риска: внешней среды, медикаментов, низкой влажности воздуха и работы на компьютере. Однако нефармакологическое лечение имеет плохой комплаенс среди пациентов, они, как правило, не выполняют назначенные процедуры. Назначение противовоспалительных средств более воспринимается пациентами.
Общие принципы лечения БСП можно подразделить на несколько основных групп:
– применение слезозаменителей;
– фармакологическая стимуляция слезопродукции;
– применение блокирования слезных точек;
– использование лечебных контактных линз;
– противовоспалительная терапия;
– применение муколитических средств;
– витамин А в лечении сухого кератоконъюнктивита;
– хирургические методы лечения;
– гигиена глаз:
• соблюдение зрительного режима (частота морганий, ограничение зрительной нагрузки и др.);
• терапевтическая гигиена век – теплые компрессы; самомассаж.
Одним из основных компонентов лечения БСП является заместительная терапия, проводимая в виде инстилляций слезозаменителей – «искусственная слеза». Принцип действия этой группы препаратов основан на восполнении дефицита водного слоя прекорнеальной слезной пленки и удержании слезной пленки в стабильном положении. Это очень важно, так как при аномалии прекорнеального слоя слезной пленки происходит нарушение смачиваемости и повреждение эпителия, что ведет к развитию дистрофических изменений роговицы и конъюнктивы, а также к стойкому хроническому дискомфорту у больных.
Начиная с XIX века, в качестве препаратов искусственной слезы стали использовать водные растворы поваренной соли, раствор Рингера, водные растворы глицерина и различные масла. Несколько десятилетий назад в терапии ССГ стали отдавать предпочтение природным полимерам, а именно сыворотке аутокрови, сухой плазме и другим. В связи со сложностью производства и недостаточной эффективностью данных препаратов они были заменены искусственными полимерами.
Современные препараты представляют собой водные растворы гидрофильных биологически инертных полимеров (производные метилцеллюлозы, поливиниловый спирт, поливинилпирролидон, полиакриловая кислота, карбомер, гиалуроновая кислота и др.) с включением различных консервантов и неорганических солей. Для достижения желаемого эффекта упомянутые препараты ежедневно инстиллируют в больной глаз с периодичностью до 6 раз в сутки. Терапия проводится перманентно на протяжении многих лет жизни пациента.
Отдельные авторы считают, что применение некоторых препаратов искусственной слезы вызывает гипотонию клеток и изменение осмолярности слезы при использовании ее заменителей. Большая часть современных препаратов искусственной слезы имеет осмолярность ниже физиологической нормы (от 200 до 260 mOsm/1). Это положительно влияет на регуляцию гидратирования тканей, микрокистозный отек и адгезию эпителия с подлежащей стромой. В связи с этим было выдвинуто положение об обязательном измерении осмолярности слезы для определения оптимальной концентрации вводимого раствора с целью создания прочной прекорнеальной пленки.
Исследования Холи с соавторами показали, что даже закапывание гипотонического раствора снижает осмолярность слезы через 1 минуту после инстилляций с 300-311 mOsm/1 до 285 mOsm/1.
В состав препаратов искусственной слезы входят также консерванты: бензалконий хлорид, хлорбутанол, хлоргексидин и др. Так как консерванты оказывают токсическое действие на поверхность роговицы, в связи с этим разрабатываются препараты искусственной слезы без консервантов. Применение препаратов без консервантов снижает десквамацию клеток роговичного эпителия. В настоящее время широко применяются глазные капли, помещенные в систему «Комод» (Урсафарм, Германия), которая представляет собой герметичное дозаторное устройство, позволяющее хранить растворы без консервантов – это пролонгированные слезозаменители Хило-комод, Хиломакс-комод и др.
Для поддержания постоянства электролитного состава, величины pH (7,2-7,5) и осмолярности (150-300 мосм/л) в состав препаратов входят микроэлементы и буферные системы.
Основным недостатком препаратов искусственной слезы на водной основе являлась необходимость их частых инстилляций. В некоторых случаях, из-за недостаточной вязкости, препараты этой группы не формировали качественную слезную пленку. В последнее время широко применяются препараты искусственной слезы на гелевой основе, которые обладают пролонгированным действием и в то же время из-за большей вязкости могут формировать более устойчивую слезную пленку при неровностях роговицы.
При отсутствии ожидаемого терапевтического эффекта целесообразно применение комбинированной терапии из двух препаратов с различной вязкостью.
Выбор препарата искусственной слезы осуществляют, ориентируясь на показатели стабильности слезной пленки и субъективные ощущения больных на фоне проводимой терапии. В дальнейшем оптимальный для каждого конкретного больного препарат или комбинацию препаратов инстиллируют с частотой в зависимости от чувства дискомфорта пациента.
Следует отметить, что последнее время большое внимание стали уделять механизму действия слезозаместительного препарата. Так, отдельные слезозаменители замещают муциновый слой слезной пленки (Офтагель, Визин чистая слеза), следовательно, их назначение оправдано при муцинодефицитной форме «сухого глаза», также разрабатываются слезозаместительные препараты, замещающие липидный компонент слезной пленки.
Помимо применения препаратов искусственной слезы, для стабилизации прекорнеального слоя и разработки способов пролонгирования их действия неоднократно предпринимались попытки воздействия непосредственно на процесс слезоотделения. Ограничение показаний к их применению связаны с необходимостью существования условий резервных возможностей слезопродукции. Наличие кардиоваскулярных и гастроинтестинальных побочных реакций после применения раствора пилокарпина снизило показания для использования этого препарата в целях стимуляции слезопродукции. К стимуляторам относятся бромгексин и элоизин, применение которых ограничено из-за раздражающего действия на ткани роговицы. Последние исследования на животных моделях предполагают наличие многоступенчатого нейромодуляторного механизма управления секреции слезы. Эти данные могут сформировать новое направление в поиске препаратов, регулирующих слезопродукцию.
Исходя из того что в нормальных условиях слезная жидкость оттекает из глаза через слезные пути в полость носа, одним из методов лечения ССГ, с целью сохранения слезной секреции, применялись различные способы блокирования слезных точек: прижигание, введение желатина или различных клейких тканей, таких как, например, N-бутил цианоакрила непосредственно в слезные канальцы. В качестве имплантатов используют жесткие силиконовые обтуранты (Feeeman J.M., 1975), которые вводят в канальцы с помощью пинцетов или проводников. Силиконовые обтуранты удерживаются в канальцах в течение многих месяцев. При необходимости они могут быть извлечены. Все эти методы имели один существенный недостаток – полное выключение слезовыводящих путей.
В настоящее время с целью обтурации слезоотводящих путей применяются коллагеновые заглушки. Продолжительность их действия ограничена 5-7 сутками, в течение которых происходит постепенное растворение коллагена. Также используется ношение герметизирующих очков. В их конструкцию дополнительно введена плотная водонепроницаемая панель, которая крепится к оправе и плотно прилегает к коже лица. Кроме того, к внутренней поверхности этой панели может быть прикреплена губчатая ткань, предназначенная для периодического увлажнения водой.
При поражении роговицы при БСП (дистрофические изменения, нитчатый и буллезно-нитчатый кератит, а также кератопластические операции) возникает необходимость защиты ее от неблагоприятных воздействий внешней среды, способствующих усилению процесса испарения влаги с поверхности глаза, с одной стороны, и созданию условий для восстановления эпителиального покрова и улучшения зрительных функций, с другой. С этой целью применяются лечебные контактные линзы.
К использованию контактных линз относятся достаточно осторожно в связи с возможным риском развития инфекционных осложнений, хотя их эффективность подтверждена при нитчатом кератите. Доказана возможность использования и определены оптимальные сроки ношения высокогидрофильных 70% лечебных мягких контактных линз (МКЛ) как симптоматического средства в лечении тяжелых форм проявления сухого кератоконъюнктивита для достижения эпителизации и зрительной реабилитации. По клиническим наблюдениям, в сроки до 10 дней, как правило, заканчивается эпителизация поверхности роговицы и происходит дальнейшее постепенное повышение остроты зрения на 0,2-0,3. При этом максимальное снижение скорости потребления кислорода роговицей глаза с 70% МКЛ происходит в первые сутки и составляет 27%. В течение последующей недели происходит адаптация и повышение скорости потребления кислорода на 3% и стабилизация этого показателя.
Одним из методов лечения БСП является применение кортикостероидов. Вообще, применение кортикостероидов и антиметаболитов в лечении кератоконъюнктивита Сикка нежелательно. Однако при других состояниях, таких как пемфигоид и синдром СтивенсаДжонса, их применение может быть эффективным. В любом случае их применение требует системного контроля.
У ряда пациентов с БСП для клинической картины характерно наличие застойной слизи в виде нитей или сгустков муцина.
Вязкость муцина снижается при использовании 10% или 20% ацетилцистеина. Однако этот препарат обладает раздражающим действием.
Как правило, проводится сочетанная терапия БСП. Так, альтернативная схема лечения СКК (в том числе при лечении синдрома Съегрена) предложена Т.Н. Сафоновой. В зависимости от стадии заболевания автор предлагает применение слезозаменителей, дезинфицирующих средств, витамина А, электрофореза лизоцима из среды 10% димексида на область слезной железы, окклюзии слезных точек силиконовой заглушкой, применение 70% высокогидрофильных лечебных мягких контактных линз.
При недостаточной эффективности консервативной терапии используют хирургические методы лечения, в частности, пластику конъюнктивой по Кунту и амниопластику. Как правило, хирургическое лечение проводится на фоне консервативных методов лечения при тяжелых формах ССГ.
Таким образом, существует большое количество способов лечения БСП. При выборе метода и объема лечения исходят из этиологии и патогенеза развития нарушений слезной пленки. С развитием хирургии, в частности, кератопластики, актуальность приобретает изучение особенностей патогенеза и подхода к лечению БСП как при фоторефракционных операциях, так и при любых других полостных операциях, связанных с повреждением поверхности глаза, включая экстракцию катаракты, антиглаукомные операции, витреоретинальные вмешательства и т.д. Разрабатываются специальные инструменты и техники операций на мейбомиевых железах (например, Митчелл Джексон, США) (рис. 7).
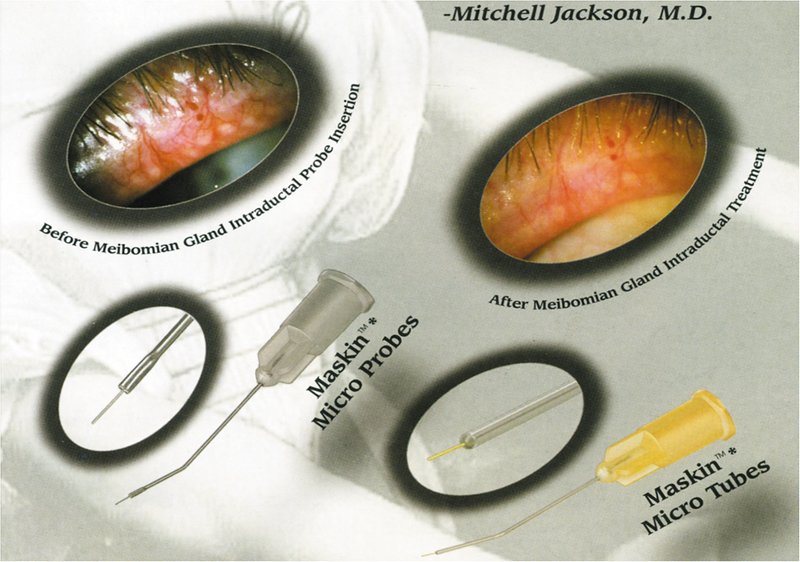
Рис. 7. Микротубы Маскина (США) для внутрипротокового дренажа
мейбомиевых желез
Конечно, хирургические методы лечения могут применяться в особенно тяжелых случаях. Такие случаи, к счастью, встречаются нечасто и составляют около 1% от общего числа пациентов с болезнью слезной пленки. Все остальные пациенты показывают хорошие результаты лечения при применении несложных способов терапевтической гигиены век с помощью специальных средств. Однако следует помнить и настойчиво объяснять пациентам, что хороший терапевтический эффект достигается только при хорошем комплаенсе. То есть только тогда, когда пациент неукоснительно регулярно и ежедневно проводит профилактические гигиенические и лечебные процедуры для век, которые назначил врач.
Итак, особое место в лечении пациентов с болезнью слезной пленки отводится гигиене глаз, которая включает соблюдение зрительного режима и терапевтическую гигиену век.
Врач-офтальмолог должен не только правильно диагностировать изменения со стороны слезопродуцирующей системы, но и, самое главное, объяснить пациенту насколько сильно зависит эффективность проводимого лечения от соблюдения самим пациентом зрительного режима и регулярного проведения терапевтической гигиены век.
Соблюдение зрительного режима включает субъективные факторы – при повышенной зрительной нагрузке (работа у компьютера, вождение автомобиля и др.) увеличивать число морганий, что позволит эффективно обновлять слезную пленку, делать перерывы в работе, по возможности выходить на свежий воздух, проветривать помещение и увлажнять воздух.






