24 ноября в Москве состоялся очередной Пироговский офтальмологический форум. В торжественном открытии приняли участие академик РАН, генеральный директор Национального медико-хирургического центра им. Н.И. Пирогова О.Э. Карпов, академик РАН, главный внештатный специалист-офтальмолог Минздрава РФ, директор ФГБУ «НМИЦ глазных болезней им. Гельмгольца» В.В. Нероев, генеральный директор ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» к.м.н. Д.Г. Арсютов.
С почетными докладами выступили главный офтальмолог Пироговского центра профессор М.М. Шишкин, тема его доклада «НМХЦ им. Н.И. Пирогова. Центр офтальмологии», и заместитель генерального директора ФГАУ «НМИЦ «МНТК «Микрохирургия глаза» им. акад. С.Н. Федорова» по организационно-методической работе профессор Н.С. Ходжаев, представивший доклад «Сквозные процессы как инструмент управления деятельности медицинской организации».
Секция «Инновации в витреоретинальной хирургии»
Открыл работу секции профессор А.Д. Чупров (Оренбург), сделавший доклад на тему «Анализ выбора тактики внутриглазного вмешательства». Цель исследования заключалась в проведении сравнительного анализа клинико-функциональных результатов одномоментной ФЭК с первичной витрэктомией и двухэтапной операции на примере 6749 случаев за период с 2019 по 2023 год.
Исследование проводилось по следующим анализируемым признакам: хирург, возраст пациента, суммарное поле зрения, динамика поля зрения, наличие рецидивов в п/о периоде, наличие фибрина, офтальмогипертензии; вторичная глаукома.
Полученные результаты позволили авторам прийти к следующим выводам. При оценке эффективности методов лечения необходим комплексный подход, основанный на рациональном знании, подкрепленном данными статистики. Предположение о влиянии большого объема хирургического вмешательства при одномоментной ФЭК с первичной витрэктомией на развитие рецидивов и появление фибрина в п/о периоде не подтверждается результатами данного исследования. Вероятность развития офтальмогипертензии и вторичной глаукомы после одномоментного вмешательства достоверно ниже, чем после двухэтапной операции.
«Распространенность и хирургическое лечение отслойки сетчатки при близорукости высокой степени» — тема сообщения профессора А.Н. Самойлова (Казань). Докладчик обратил внимание на ряд факторов, влияющих на рост отслойки сетчатки (ОС) у миопов. Это более молодой возраст, большее осевое удлинение, приводящее к усилению периферического истончения сетчатки и периферической патологии сетчатки, повышенные перпендикулярные и тангенциальные тракционные силы в заднем полюсе стафиломатозного глаза, приводящие к миопической тракционной макулопатии, фовеошизису, макулярному отверстию и фовеальной ОС.
Риск ОС при миопии высокой степени (МВС) пропорционален осевой длине и сферическому эквиваленту (СЭ). Без хирургического вмешательства пожизненный риск ОС при МВС в 20 раз выше, чем при эмметропии. Риск ОС еще более возрастает у пациентов с МВС после операции по удалению катаракты.
Наиболее распространенными хирургическими методами в лечении макулярной отслойки и отслойки сетчатки при МВС являются метод перевернутого лоскута внутренней пограничной мембраны (ВПМ), применение богатой тромбоцитами плазмы. При выполнении этих процедур рекомендуется оставление лоскута ВПМ в области вокруг желтого пятна.
Профессор И.В. Зольникова (Москва) сделала доклад на тему «Электрофизиологические исследования при наследственных заболеваниях органа зрения». Электрофизиологические исследования (ЭФИ) – это тесты, измеряющие реакцию на свет различных структур глаза и зрительной системы. Для ЭФИ характерны неинвазивность, объективность, количественная оценка. Применяются для оценки дисфункции ретинального пигментного эпителия (РПЭ), сетчатки, макулы, зрительного нерва, хиазмы, вышележащих отделов зрительного анализатора.
ЭФИ в научных исследованиях используются в глубоком фенотипировании наследственных заболеваний, в разработке лекарственных препаратов, ключевых методов лечения заболеваний, угрожающих зрению.
Основными составляющими ЭФИ в диагностике наследственных заболеваний глаз являются электроретинография (ЭРГ), зрительные вызванные потенциалы (ЗВП), электроокулография (ЭОГ).
Опыт НМИЦ ГБ им. Гельмгольца показывает, что в структуре наследственных заболеваний сетчатки около половины случаев составляет пигментный ретинит, четверть – болезнь Штаргардта.
ЭФИ широко используются в детской практике, особенно в дифференциальной диагностике нистагма, слабовидения, для выявления амавроза Лебера, некоторые формы которого являются излечимыми.
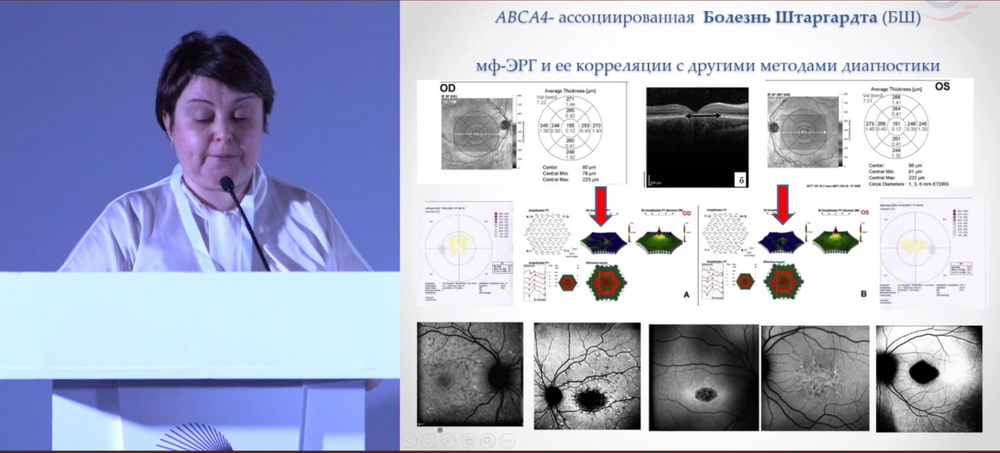
Мультифокальная ЭРГ позволяет оценивать макулярную функцию. На рис. 1 представлено клиническое применение метода при болезни Штаргардта. Макулярная хроматическая ЭРГ и паттерн-ЭРГ также позволяют оценивать функцию в макулярной области.
Электрофизиологические методы позволили выявить такие заболевания, как KCNV2-ассоциированная колбочковая дистрофия с супернормальной палочковой ЭРГ, синдром усиления функции S-колбочек NR2E3, брадиопсия. Брадиопсия представляет собой синдром стационарной дисфункции колбочек, дебютирует в раннем детстве, сопровождается легкой светобоязнью, значительно замедленной темновой и световой адаптацией, умеренным снижением остроты зрения. Для заболевания характерны нормальное светоощущение, трудности наблюдения за движущимися объектами, отсутствие изменений на глазном дне.
Электрофизиологические методы используются для оценки эффективности генной терапии. Важным методом диагностики функции пигментного эпителия на различных стадиях болезни Беста является электроокулография.
Зрительные вызванные потенциалы (ЗВП) позволяют установить заболевания зрительного нерва, в частности, нейропатию Лебера, однако не позволяют дифференцировать между наследственной и ненаследственной этиологией.
Подводя итог докладу, профессор И.В. Зольникова напомнила, что ЭФИ являются объективными, неивазивными методами оценки зрительных функций, позволяют установить распространенность, степень и клеточную природу (локализацию) дисфункции; дифференцировать поражения сетчатки и зрительного нерва/зрительного пути; оказывают помощь в более доказательной консультации относительно прогноза заболевания (болезни Штаргардта); имеют важное значение для дифференциальной диагностики нистагма и слабовидения с рождения и в раннем детском возрасте (амавроз Лебера, ахроматопсия, врожденная стационарная ночная слепота); являются патогномоничными для некоторых заболеваний.
К.м.н. С.В. Сосновский (Санкт-Петербург) от группы авторов представил доклад на тему «Эффективность аутотранслокации пигментного эпителия сетчатки в лечении рубцовой стадии неоваскулярной ВМД». Золотым стандартом лечения неоваскулярной ВМД является антиангиогенная терапия. Одним из состояний, при которых антиангиогенная терапия неэффективна, является субретинальный фиброз – исход заболевания с формированием под макулярной сетчаткой грубого фиброзного рубца. Субретинальный фиброз сопровождается положительной центральной скотомой, эксцентричным зрением, слабовидением, значительным ухудшением качества жизни. С морфологической точки зрения – это отсутствие пигментного эпителия, наличие патологического субстрата между нейросенсорной сетчаткой (НСС) и сосудистой оболочкой, утрата хориокапиллярного слоя, дегенеративные изменения НСС (неустранимое состояние), атрофия НСС (неустранимое состояние). Отсутствие пигментного эпителия и патологический субстрат – состояния устранимые, благодаря предложенной G.A. Peyman в 1991 году методике субретинального вмешательства с пересадкой пигментного эпителия сетчатки.
Классическими показаниями для аутотранслокации ПЭС являются свежее гигантское субретинальное макулярное кровоизлияние, субфовеолярный разрыв; вторичные показания, для которых характерны значительные сроки процесса и низкий функциональный прогноз, ‒ резистентная СНМ с высокой активностью, субретинальное макулярное кровоизлияние, субретинальный макулярный фиброз в исходе неоваскулярной ВМД.
Цель работы заключалась в анализе безопасности и эффективности аутотранслокации пигментного эпителия сетчатки при рубцовой стадии неоваскулярной ВМД. В исследовании приняли участие 22 пациента (5 мужчин и 17 женщин).
Материалы и методы: офтальмоскопия, фоторегистрация, ОКТ, визометрия. Безопасность вмешательства оценивали по критерию развития осложнений в п/о периоде. 59% вмешательств не имели осложнений, в 41% ‒ различные осложнения, в т.ч. ПВР, отслойка сетчатки (7 случаев: 5 – обратимых, 2 ‒ необратимых), эпиретинальный фиброз (1 случай – отказ от продолжения лечения), макулярный разрыв (2 обратимых случая).
В группу оценки эффективности вошло 16 пациентов. Острота зрения у 9 пациентов незначительно улучшилась, у 3 – не изменилось, у 4 пациентов наблюдалось ухудшение к концу периода наблюдения. Максимальное улучшение составило 0,12, максимальное ухудшение ‒ -0,05.
Морфология: наличие ПЭС под фовеа – 100%; правильная ориентация лоскута ПЭС – 100%; отсутствие патологической жидкости – 100%; отсутствие отека НСС – 88%; отсутствие отека лоскута ПЭС – 88%; наличие фовеолярной ямки – 37%.
Таким образом, хирургия обеспечивает восстановление максимально «приближенных к нормальным» макулярных анатомических взаимоотношений тканей, устранение ХНВ, устранение «фиброзной прослойки» между НСС и сосудистой оболочкой, а также создание условий для функциональной активности сетчатки.