Ретинальная ангиоматозная пролиферация (РАП)
Если обратиться к истории вопроса, то впервые РАП была описана M.E. Hartnett в 1992 г. как ретинальный сосудистый аномальный комплекс [17], в 1995 г. исследователи дополнили представление о РАП, приписав этой патологии причастность к отслойкам пигментного эпителия [18], после чего в 1996 г. описали РАП как глубокий ретинальный сосудистый аномальный комплекс [19]. В 2000 г. другая группа ученых отметила наличие ретино-ретинальных анастомозов при РАП, но подчеркнули, что этот вариант может протекать без присутствия отслойки пигментного эпителия [20]. Все представления были объединены в 2001 г., когда был признан термин «РАП» — представляющей собой форму скрытой ХНВ, связанной с пролиферацией интраретинальных капилляров в парамакулярной области и формированием телеангиоэктазий [21].
Данные по частоте встречаемости РАП различны — некоторые ученые полагают, что РАП встречается примерно в 10-12% случаев впервые выявленных неоваскулярных поражений [22], в других исследованиях показано, что частота встречаемости РАП достигает 21%, при этом ретинальные анастомозы были выявлены у 23% пациентов с серозной отслойкой ПЭ, в то время как у 13% больных они диагностированы у пациентов без отслойки ПЭ [20].
Следует отметить результаты одного из гистопатологических исследований девяти неоваскулярных поражений класса РАП, в котором авторы обнаружили только интраретинальную неоваскуляризацию в случаях со 2-й стадией, а в глазах с 3-й стадией поражения выявлена хориоидальная и интраретинальная неоваскуляризация, что совпадало с классификацией L.A. Yannuzzi (2001 г.). Кроме того, было установлено наличие экспрессии VEGF (в интраретинальной неоваскуляризации и в пигментном эпителии), CD68 — позитивных макрофагов (в зоне неоваскуляризации) и экспрессия гипокси-зависимого фактора альфа 1 и альфа 2 (HIF 1 alpha и 2 alpha) в неоваскулярных эндотелиальных клетках [23]. Эти данные подтверждали тот факт, что интраретинальная неоваскуляризация появляется до хориоидальной неоваскуляризации и ассоциирована с ишемией и увеличением экспрессии VEGF и воспалительных факторов [7, 23].
РАП преобладает у пациентов европеоидной расы женского пола, не выявляется у лиц негроидной расы и очень редко — у азиатов (около 5% среди пациентов с неоваскулярной ВМД), у последних мужчины страдают данной патологией чаще, чем женщины [21, 24-26].
Особенности ее клинического течения представлены на рис. 7 и заслуживают отдельного внимания.
В 2001 г. Lawrence A. Yannuzzi предложил классификацию ретинальной ангиоматозной пролиферации по стадиям, которая наиболее широко применяется в настоящее время [21]:
• I стадия — интраретинальная неоваскуляризация — пролиферация интраретинальных капилляров из глубоких капиллярных сплетений в парамакулярной области. Эта стадия часто сопровождается интраретинальными кровоизлияниями и отеком.
• II стадия — субретинальная неоваскуляризация, когда интраретинальная неоваскуляризация распространяется за слой фоторецепторов в субретинальное пространство. Появляется локальная отслойка нейросенсорной сетчатки с признаками интраретинального отека, интраретинальных и преретинальных кровоизлияний, а также характерными серозными отслойками пигментного эпителия:
• IIА — без отслойки пигментного эпителия;
• IIБ — с отслойкой пигментного эпителия.
• III стадия — ретино-хориоидальная неоваскуляризация, видимая клинически и ангиографически, иногда сопровождающаяся геморрагической ОПЭ. На этой стадии происходит формирование ретинально-хориоидальных анастомозов.
D. Gass (2003) предложил классификацию РАП [27], в которой выделено не три, а пять стадий процесса, из которых следует обратить внимание на первые две:
1) Преклиническая стадия. Ат-рофия наружных слоев сетчатки, ретинальные капилляры, подходящие к хориоидальному неоваскулярному комплексу под ПЭ. Признаков ретинально-хориоидальных анастомозов нет;
2) Ранние клинические признаки. Анастомозы между расширенными капиллярами в глубоких слоях сетчатки и хориоидальный неоваскулярный комплекс, ассоциированный с мелкими интраретинальными кровоизлияниями, которые служат первыми признаками хориоретинальных анастомозов.
На наш взгляд, для диагностики данной формы неоваскуляризации следует рассматривать клинико-инструментальные, а точнее — клинико-ОКТ параллели.
Клинические проявления РАП включают ретинальные и преретинальные кровоизлияния, а также отслойки нейросенсорной сетчатки и пигментного эпителия с субретинальными кровоизлияниями. Кровоизлияния при этой форме ХНВ обычно мелких размеров и могут находиться сразу в нескольких местах [28].
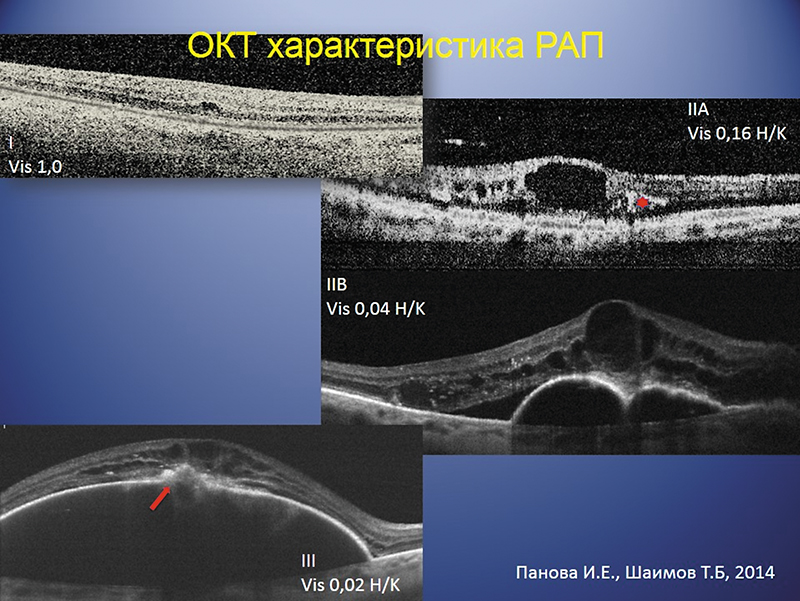
Основные ОКТ-признаки РАП представлены на рис. 8.
При проведении ОКТ в I стадии РАП выявляется фокальная область повышения интраретинальной рефлективности, обычно экстрафовеальной локализации, не связанной с другими эпи- , интра- и субретинальными изменениями толщины сетчатки. Если интраретинальные кровоизлияния присутствуют, они могут быть неразличимы, при этом на ОКТ появляются участки гиперрефлективности. Появление интраретинальной или субретинальной жидкости на ОКТ следует рассматривать как признак прогрессирования РАП. Макулярный отек представлен хорошо видимыми сливными интраретинальными гипорефлективными полостями, которые граничат с наружной сетчаткой в экстрафовеальной области, увеличивают общую толщину сетчатки в центре фовеа и разделяются между собой рефлективными септами. Во II стадии процесса на ОКТ отслойка нейросенсорной сетчатки представлена гипорефлективным участком между нейросенсорной фовеальной сетчаткой и ПЭ. Прогрессирование данной стадии процесса сопровождается увеличением количества и размеров интраретинальных кистовидных полостей, образованием серозной отслойки ПЭ вследствие субретинальной неоваскуляризации. По мере прогрессирования РАП и образования хориоидальной неоваскуляризации латеральный рост и высота элевации ПЭ, а также гипорефлективные полости (интра- и субретинальные жидкости), могут приобретать более выраженный характер. Из-за невозможности отличить новообразованные, активно пролиферирующие сосуды от рубцовой ткани и четкого изображения структур под отслойкой ПЭ на ОКТ затруднительно просчитывать протяженность зоны неоваскуляризации, а также с достоверной точностью дифференцировать II стадию (субретинальную неоваскуляризацию) от III стадии (хориоидальной неоваскуляризации). В отдельных случаях возможно идентифицировать хориоретинальный анастомоз (звездочка, стрелка).
Диагностика РАП при проведении в/в ФАГ часто вызывает затруднения: на ФАГ-картине можно увидеть скрытую ХНВ с неопределенной зоной точечных гиперфлюоресценций, более отчетливо видную на поздних стадиях [21]. Так же, как и при ПХВ, ICG ангиография является более достоверным методом для выявления данной патологии, чем ФАГ. РАП можно определить на средних или поздних фазах ангиографии как локальные зоны гиперфлюоресценции на окончаниях ретинальных сосудов, так называемые «горячие точки». Также отмечено характерное просачивание жидкости в окружающие ретинальные и субретинальные пространства [28, 29].
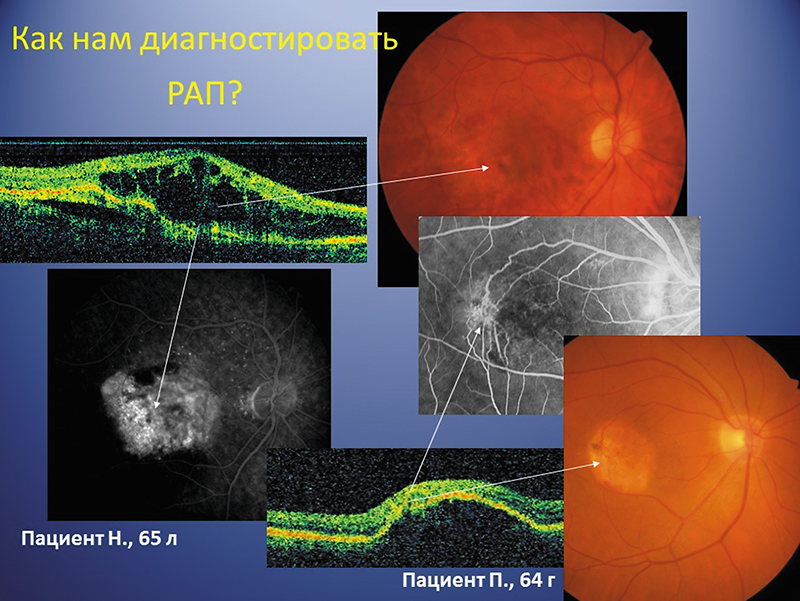
Представленные на рис. 9 клинические примеры позволяют нам диагностировать данный подтип неоваскулярной ВМД (РАП, IIБ стадия) на основе сопоставления клинической, флюоресцентно-ангиографической и ОКТ-картины.
Таким образом, на основе анализа собственных клинических наблюдений и актуального литературного материала, посвященного данной проблеме, нами рассмотрены основные вопросы, касающиеся диагностики подтипов неоваскуляризации при ВМД — полипоидной хориоидальной васкулопатии и ретинальной ангиоматозной пролиферации. Целесообразность определяется обоснованием выбора метода лечения, поскольку традиционные режимы анти-VGF терапии оказываются малоэффективными. Мы надеемся, что данный материал окажется полезным для практикующих врачей-офтальмологов и поможет в дифференциальной диагностике и определении тактики лечения такого сложного заболевания, как возрастная макулярная дистрофия.
Литература
1. Koreen L, Hollar MW, Cousin S. Where Do PCV and RAP Fit in the Spectrum of AMD CNV Subtypes? Determining lesion morphology provides for better diagnosis and treatment. Retinal Physician 2010 Oct.
2. Cohen SY, Creuzot-Garcher C, Darmon J, Desmettre T, Korobelnik JF, Levrat F, Quentel G, Palis S, Sanchez A, de Gendre AS, Schluep H, Weber M, Delcourt C. Types of choroidal neovascularisation in newly diagnosed exudative age-related macular degeneration. Br J Ophthalmol. 2007 Sep; 91 (9):1173-6.
3. Yannuzzi LA, Sorenson J, Spaide RF, Lipson B. Idiopathic polypoidal choroidal vasculopathy (IPCV). Retina 1990; 10:1-8.
4. Lim TH, Laude A, Tan CS. Polypoidal choroidal vasculopathy: an angiographic discussion. Eye (Lond). 2010 Mar; 24 (3):483-90.
5. Sho K, Takahashi K, Yamada H, et al. Polypoidal choroidal vasculopathy: incidence, demographic features, and clinical characteristics. Arch Ophthalmol 2003 Oct; 121 (10):1392-6.
6. Cackett P, Yeo I, Cheung CM, Vithana EN, Wong D, Tay WT, Tai ES, Aung T, Wong TY. Relationship of smoking and cardiovascular risk factors with poly-poidal choroidal vasculopathy and age-related macular degeneration in Chinese persons. Ophthalmology. 2011 May; 118 (5):846-52.
7. Ueta T, Obata R, Inoue Y, Iriyama A, Takahashi H, Yamaguchi T, Tamaki Y, Yanagi Y. Background comparison of typical age-related macular degeneration and polypoidal choroidal vasculo-pathy in Japanese patients. Ophthalmo-logy. 2009 Dec; 116 (12):2400-6.
8. Hirami Y, Tsujikawa A, Otani A, Yodoi Y, Aikawa H, Mandai M, Yoshi-mura N. Hemorrhagic complications after photodynamic therapy for polypoidal choroidal vasculopathy. Retina. 2007 Mar; 27 (3):335-41.
9. Sakurada Y, Yoneyama S, Imasawa M, Iijima H. Systemic risk factors associ-ated with polypoidal choroidal vasculopathy and neovascular age-related macular degeneration. Retina. 2013 Apr; 33 (4):841-5.
10. Toyama T, Ohtomo K, Noda Y, Ueta T. Polypoidal choroidal vasculopathy and history of central serous chorioretinopathy. Eye (Lond). 2014 Aug; 28 (8):
992-7.
11. Mori K, Horie-Inoue K, Gehlbach PL, et al. Phenotype and genotype characteristics of age-related macular dege-neration in a Japanese population.
Ophthalmology 2010; 117:928-938.
12. Liang, X.Y., Lai, T.Y., Liu, D.T. et al. Differentiation of exudative age-related macular degeneration and polypoidal choroidal vasculopathy in the ARMS2/HTRA1 locus. Invest Ophthalmol Vis Sci. 2012; 53: 3175—3182.
13. Tong JP, Chan WM, Liu DT, et al. Aqueous humor levels of vascular endothelial growth factor and pigment epitheliumderived factor in polypoidal choroidal vasculopathy and choroidal neovascularization. Am J Ophthalmol. 2006 Mar; 141 (3):456-62.
14. Kikuchi, M., Nakamura, M., Ishikawa, K. et al. Elevated C-reactive protein levels in patients with polypoidal choroidal vasculopathy and patients with neovascular age-related macular dege-neration. Ophthalmology. 2007; 114: 1722—1727.
15. Spaide RF, Yannuzzi LA, Slakter JS, et al. Indocyanine green video angiography of idiopathic polypoidal choroidal vasculopathy. Retina 1995;15:100-10.
16. Imamura Y, Engelbert M, Iida T, et al. Polypoidal choroidal vasculopathy: A review. Surv Ophthalmol. 2010 NovDec; 55 (6):501-15.
17. Hartnett ME, Weiter JJ, Gardts A, Jalkh AE. Classification of retinal pigment epithelial detachments associated with drusen. Graefes Arch Clin
Exp Ophthalmol 1992;230:11-19.
18. Kuhn D, Meunier I, Soubrane G, Coscas G. Imaging of chorioretinal anastomoses in vascularized retinal pigment epithelium detachments. Arch Ophthalmol. 1995; 113:1392—1398.
19. Hartnett ME, Weiter JJ, Stauren-ghi G, Elsner AE. Deep retinal vascular anomalous complexes in advanced age-related macular degeneration. Ophthalmology 1996;103:2042—2053.
20. Slakter JS, Yannuzzi LA, Schneider U, et al. Retinal choroidal anastomoses and occult choroidal neovascularization in age-related macular degeneration. Ophthalmology 2000; 107:742-754.
21. Yannuzzi LA, Negro S, Iida T, Car-valho C, Rodriguez-Coleman H, Slakter J, Freund KB, Sorenson J, Orlock D, Borodoker N. Retinal angiomatous proliferation in age-related macular degeneration. Retina 2001; 21: 416-34.
22. Freund KB, Klais CM, Eandi CM, et al. Sequenced combined intravitreal triamcinolone and indocyanine green angiographyguided photodynamic therapy for retinal angiomatous proliferation. Arch Ophthalmol. 2006 Apr;124 (4):487-92.
23. Shimada H, Kawamura A, Mori R, Yuzawa M. Clinicopathological findings of retinal angiomatous proliferation. Graefes Arch Clin Exp Ophthalmol. 2007; 245 (2): 295-300.
24. Liu Y, Wen F, Huang S, et al. Subtype lesions of neovascular age-related macular degeneration in Chinese patients.Graefe’s Arch Clin Exp Ophthalmol. 2007;10:1441-5.
25. Maruko I, Iida T, Saito M, Nagayama D, Saito K. Clinical characteristics of exudative age-related macular degeneration in Japanese patients. Am J Ophthalmol. 2007; 144:15-22, 24.
26. Donati MA, Carifi G, Virgili G, Menchini U. Retinal angiomatous proliferation: association with clinical and angiographic features. Ophthalmolo-gica. 2006; 220:31-6.
27. Gass JDM, Agarwal A, Lavina AM, Tawasky KA. Focal inner retinal hemorrhages in patients with drusen: an early sign of occult choroidal neovascula-rization and chorioretinal anastomosis. Retina 2003; 23:741-751.
28. Fernandes LH, Freund KB, Yannu-zzi LA, et al. The nature of focal areas of hyperfluorescence of “hot spots” imaged with indocyanine green angiography. Retina. 2002 Oct;22 (5):557-68.
29. Politoa A, Napolitano MC, Bandello F, Chiodini RG. The role of optical coherence tomography (OCT) in the diagnosis and management of retinal angiomatous proliferation (RAP) in patients with age-related macular degeneration. Ann Acad Med Singapore. 2006 Jun; 35 (6):420-4.
Страницы: 1 2