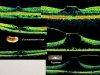
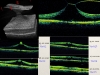
Зато на ОКТ (рис. 5) хорошо становятся видны трансформации КМК при его расслоении под действием сагиттальных или тангенциальных тракций. При этом при преобладании сагиттального вектора тракции за счет конденсации клеточных и волокнистых структур уплотняется широкое основание КМК, и в направлении стекловидного тела вырастает оптически практически пустое трапециевидное образование, напоминающее по виду гору Фудзияму. При преобладании тангенциальных векторов тракции на КМК в нем возникают 2 зоны оптической разреженности — у вершины конуса и кольцевидная зона у его основания. На оптическом срезе ОКТ, таким образом, возникает фигура, напоминающая «хэллоуинскую» тыкву. Однако при более тщательном рассмотрении внутри этих «полостей» можно увидеть пусть и разреженную, но структурность.
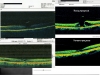
Дальнейший ход естественного развития макулярного тракционного синдрома и сопутствующего макулошизиса определяется индивидуальной прочностью КМК на разных уровнях от основания до вершины. Чаще всего происходит отрыв широкого основания конуса, прикрепленного собственно к стекловидному телу, и смещение этого оторванного основания вовнутрь глаза. То есть возникает эффект «хвоста ящерицы», когда рептилия для самосохранения жертвует своей частью. Благодаря этому механизму миллионы людей, не зная об этом, «проходят мимо» формирования макулярного отверстия, по сути, по краю пропасти (на рис. 6 два изображения слева — снизу вверх).
Однако так везет не всем. У тех людей, у которых механическая прочность КМК от основания до вершины превышает определенный предел, стекловидное тело «выдирает» из тела фовеолы центральный стержень конуса с формированием сквозного макулярного отверстия.
Иногда томографическая картина выраженного передне-заднего растяжения фовео-лы может держаться довольно долго (более полугода), заканчиваясь, тем не менее, чаще всего формированием сквозного макулярного отверстия.
В случае преобладания тангенциально направленных векторов тракционного воздействия (чаще на фоне произошедшей заднегиалоидной отслойки в фовеолярной области сетчатки и формирования эпиретинальной мембраны) широкое основание конуса начинает разрушаться, превращая его в некое подобие полой воронки. Причем коническая стенка этой воронки не является сплошной, вследствие чего на некоторый срезах ОКТ возникает картина плоскостного «раздирания» сетчатки на 2 слоя (преимущественно в наружном плексиформном слое). То есть формируется картина образования ламеллярного макулярного отверстия.
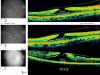
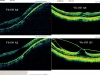
Формирование ламеллярного макулярного отверстия, в отличие от сквозного, идет весьма медленно, иногда годами. При этом очень часто у пациентов до наступления момента катастрофического падения центрального зрения, сохраняется высокий визус (рис. 7).
Хирургическое лечение тракционного макулярного синдрома, без существенной разницы реализуется он в сквозное отверстие или в ламеллярное, сводится к устранению передне-задних и тангенциальных тракций (рис. 8). При этом принципиально важно, чтобы устранение хронической тракции не сопровождалось резким ее усилением в процессе манипуляций по отделению заднегиалоидной мембраны или внутренней пограничной мембраны от собственно фовеолярной ткани. Это обеспечивается тем, что с помощью пинцета эти мембраны отделяются от ретинальной ткани только в местах, где они относительно слабо связаны с сетчаткой. Там же, где эти структуры прочно связаны друг с другом, они не разделяются «любой ценой», участки прочной взаимосвязи превращают в изолированные «острова». Такая, потерявшая механическое напряжение мембрана в течение нескольких месяцев, как правило, атрофируется. Особенно важна такая техника устранения витреоретинального натяжения в случаях значительного вытягивания фовеолярной сетчатки в сторону стекловидного тела с формированием «фудзиямоподобной» конфигурации.
Существенно облегчает интраоперационное распознавание границы «мембрана-сетчатка» применение ОКТ в режиме «on line». На рис. 9 приведен фрагмент такой операции. На этом рисунке показан пример постепенного рассасывания оставленной в ходе операции, показанной на предыдущем рисунке, эпиретинальной ткани, лишенной натяжения на поверхности сетчатки и собравшейся в комок вокруг точки прочного сращения с тканью фовеолы.
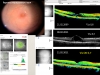
Другой пример хирургического разрешения витреотракционного синдрома (рис. 10). Слева внизу — картина ОКТ при первом появлении пациента. Справа внизу — картина через 2 года. Однако, несмотря на выраженную картину макулошизиса с формированием «псевдокистозной» полости в фовеоле, острота зрения еще сохранялась сравнительно высокой. Справа вверху показан очерченный фрагмент поверхности сетчатки, где любые тракционные воздействия на сетчатку категорически нежелательны.
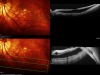
При миопии высокой степени КМК по Гассу ведет себя иначе. Мюллеровские клетки не оказывают такого механического сопротивления витреальному тракционному воздействию. Возникает картина распространенного макулошизиса. Причем на сканах ОКТ, выполненных непосредственно в фовеоле, явных признаков тракционного воздействия на сетчатку практически не видно (рис. 11). Эти тракции становятся хорошо заметными уже на границах сосудистых аркад.
Хирургическое пособие в подобных ситуациях принципиально такое же, как и при других формах витреомакулярного синдрома (рис. 12). Отличие заключается в более широкой площади пилинга эпиретинальной и заднегиалоидной мембраны — с выходом за границы сосудистых аркад (внизу картина ОКТ до операции, вверху — через 5 месяцев после).
В случае реализации витреомакулярного синдрома при миопии высокой степени в сквозное макулярное отверстие одним из рекомендуемых в литературе методов лечения является создание склерального вдавления в заднем отделе глазного яблока. В случае незакрытия отверстия после создания такого вдавления остается возможность применения витреоэктомии с расширенным по площади пилингом внутренней пограничной мембраны.
Макулошизис при комбинировании транссудативного механизма формирования интраретинальной полости вследствие возрастной макулярной дегенерации с тракционным компонентом — в ряде случаев представляется целесообразным одномоментное воздействие на оба патологические фактора — витреоэктомия с курсовым применением анти-VEGF препаратов.
Макулошизис при пролиферативной диабетической ретинопатии, как правило, имеет механическую причину и, соответственно, лечится хирургическим устранением тракционного воздействия.
Хотя при диабетическом и посттромботическом макулярных отеках преобладающим патологическим агентом является интраретинальная транссудация, и на сегодняшний день она относительно неплохо лечится курсовым применением интравитреальных инъекций анти-VEGF препаратов или кортикостериодов. При формировании диабетического или посттромботического макулярных отеков возможна комбинация транссудативного и механического компонентов. В распознавании механического компонента очень помогает ОКТ. Однако устранение механического компонента формирования макулошизиса является, как правило, весьма полезным, но недостаточным фактором лечения. Приходится держать пациента на периодической терапии интравитреальным введением анти-VEGF препаратов или стероидов.
При постувеальном макулярном отеке также чаще всего имеется комбинация транссудативного и тракционного механизмов патогенеза отека. Здесь также необходима комбинация хирургического лечения с интравитреальным введением стероидов.
Очень важно, чтобы успокаивающая плавность и неторопливость развития центрального ретиношизиса не настраивала пациента и врача на страусиную политику игры в жмурки с надвигающейся, как асфальтовый каток, проблемой, а была использована как возможность выбора оптимального момента для старта активного лечения.
Страницы: 1 2