Следовательно, офтальмологи могут перенять опыт коллег-неврологов и использовать те препараты, которые применяют они в лечении хронических нейродегенеративных заболеваний. В этом плане заслуживает внимания акатинол мемантин, который, к сожалению, не показал своей эффективности при глаукоме в 3-ю фазу клинических испытаний при многоцентровых исследованиях, в отличие от болезни Альцгеймера, при которой данный препарат был разрешен к применению комитетом FDA в США. Канадские ученые испытывали мемантин на приматах. Они взяли небольшую группу и получили впечатляющие результаты — сохранялись нейроны во всех слоях наружных коленчатых тел и коры головного мозга (слайд 2).

Слайд 2. Применение акатинол мемантина у приматов (экспериментальная модель глаукомы). Заметно сохранение нейронов наружных коленчатых тел на фоне лечения
Первая публикация на эту тему появилась в 2006 г. Еще одно важное наблюдение было предпринято N. Gupta и Y. Yucel уже на пациенте, когда наблюдали женщину 79 лет, которая при жизни болела глаукомой. Ее наблюдали 19 месяцев, это была глаукома нормального давления, и пациентка получала лечение дорзоламидом. Она умерла от вирусного миокардита. На вскрытии было обнаружено существенное уменьшение наружных коленчатых тел и зрительной коры головного мозга, аналогичное тем, что наблюдалось у приматов с экспериментальной глаукомой. Сейчас в Торонто продолжаются исследования на приматах. В 2011—2013 годах ученые стали изучать дендриты и обнаружили, что уменьшение их количества является самым ранним индикатором того, что клетка обращается в состояние апоптоза, поскольку нарушается передача информации между клетками. В публикации 2010 года, посвященной пластичности дендритов в наружных коленчатых телах, было показано, что при экспериментальной глаукоме у приматов ранее всего уменьшается количество дендритов. Следовательно, возникают перспективы лечения глаукомы на ранней стадии. В настоящее время эти исследования продолжаются.
В следующей части доклада проф. Н.И. Курышева остановилась на общих чертах патогенеза глаукомы и болезни Альцгеймера, подчеркнув, что теория протеинового мисфолдинга (т.е. нарушения правильной укладки белковой молекулы) в настоящее время рассматривается как ведущая наряду с теорией окислительного стресса, эксайтотоксического феномена и аутоиммунного воспаления. Закономерный вопрос: как часто бывает глаукома при болезни Альцгеймера. Результаты исследований по этому поводу очень противоречивы. По сути, у каждого четвертого больного болезнью Альцгеймера есть глаукома. При обоих заболеваниях выявлено отложение амилоида бета, активация каспаз, при болезни Альцгеймера увеличена ЭДЗН и имеется истончение нервных волокон сетчатки, а также нарушена транссинаптическая передача. Более того, было установлено, что даже генетические факторы, характерные для болезни Альцгеймера, обнаружены при глаукоме.
Существует ли лечение нейродегенеративной патологии в реальном мире? Ответ, к сожалению, отрицательный. Кроме акатинол мемантина, применяемого при болезни Альцгеймера, положительной информации по этому поводу пока нет.
На сегодня офтальмологам приходится рассчитывать только на то, что препараты для местного гипотензивного лечения имеют прямые нейропротекторные свойства.
Первая публикация на эту тему относится к 1996—1997 гг., когда проф. Осборн продемонстрировал в эксперименте на кроликах и в культуре изолированных ганглиозных клеток нейропротекторное действие бетаксолола. Оказалось, что этот препарат действительно повышал выживаемость ГКС при экспериментальной глаукоме. Было доказано, что он уменьшает поступление кальция в клетку, уменьшает апоптоз нейронов, и очень скоро было проведено исследование, в котором сравнили бетаксолол с тимололом и бримонидином.
О прямых нейропротекторных свойствах бримонидина за последние 10 лет было очень много публикаций, что практически сделало этот препарат номером один в лечении глаукомы.
Указанные свойства бримонидина объясняются его селективным воздействием на альфа-2-рецепторы. Именно их возбуждение приводит к комплексному воздействию на нейроны сетчатки, защищая их от апоптоза.
В 2003 г. Стефано Гандольфи провел очень интересный эксперимент на пациентах в клинике.
В двух группах больных (в одной применяли лазерную трабекулопластику, в другой — лечение бримонидином) сначала определили скорость прогрессирования глаукомы, а потом начали лечить и посмотрели, с какой скоростью будет продолжаться прогрессирование. Обнаружили, что лазерное лечение только замедляло прогрессирование, а бримонидин улучшал поля зрения. Так в клинике было получено доказательство прямого нейропротекторного действия бримонидина. Другое исследование, проведенное в США при глаукоме нормального давления, показало, что при лечении бримонидином прогрессирование было в три раза меньше, чем на тимололе, но, к сожалению, отмечались побочные действия.
Глава в одном из последних журналов «Прогресс в исследовании мозга» называется так: «Глаукома — открытое окно в нейропротекцию, нейрорегенерацию». Это означает, что на примере глаукомы возможен поиск лечения нейродегенеративной патологии. Офтальмологи должны сотрудничать с неврологами, проводить совместные исследования и симпозиумы, потому что опыт может оказаться уникальным.
Следующим докладчиком был профессор Bernhard Sabel, директор Университета нейрофизиологии и психологии Магдебургского университета (Германия). Идея пригласить проф. Sabel была продиктована тем, что в отсутствии эффективных медикаментозных нейропротекторных способов лечения метод, разработанный проф. Sabel, заслуживает внимания. Об этом свидетельствовала реакция офтальмологов на мировом конгрессе в Токио, где все доклады проф. Sabel воспринимались с большим энтузиазмом. В настоящее время проф. Sabel проводит уникальные исследования в клиниках Китая, к нему на лечение направляют своих пациентов такие известные глаукоматологи мира, как R. Ritch и R. Weinreb.
Докладчик начал с того, что подчеркнул важную роль мозга в обеспечении зрительной функции и недостаточное понимание этого аспекта офтальмологами всех стран.
В коре головного мозга, обрабатывающей зрительный сигнал, нейронов больше в 300 раз, чем в сетчатке.
Исследования с помощью МРТ показали, что у пациентов с глаукомой есть изменения в лобной доле коры головного мозга по сравнению с аналогичным отделом мозга здоровых людей такого же возраста. Был сделан вывод о том, что при нарушении зрительных функций поражается не только зрительный анализатор, но и другие области коры головного мозга.
В результате экспериментов на грызунах B. Sabel сделал вывод о том, что при сохранении 10-20% нейронов сетчатки возможно со временем восстановление до 80% зрительных функций, и это обеспечивается работой головного мозга. При глаукоме участки серого цвета, заметные при периметрии, отражают работу нейронов со сниженной зрительной функцией, но еще живых. Это области резидуального (остаточного) зрения.
Сутью восстановления функций указанных нейронов является синхронизация волн в коре головного мозга. Проследить за этим можно с помощью электроэнцефалографии. При использовании специального шлема с датчиками можно увидеть взаимосвязь работы разных центров в мозге и понять, синхронизированы они или нет в своих функциях (слайд 3).
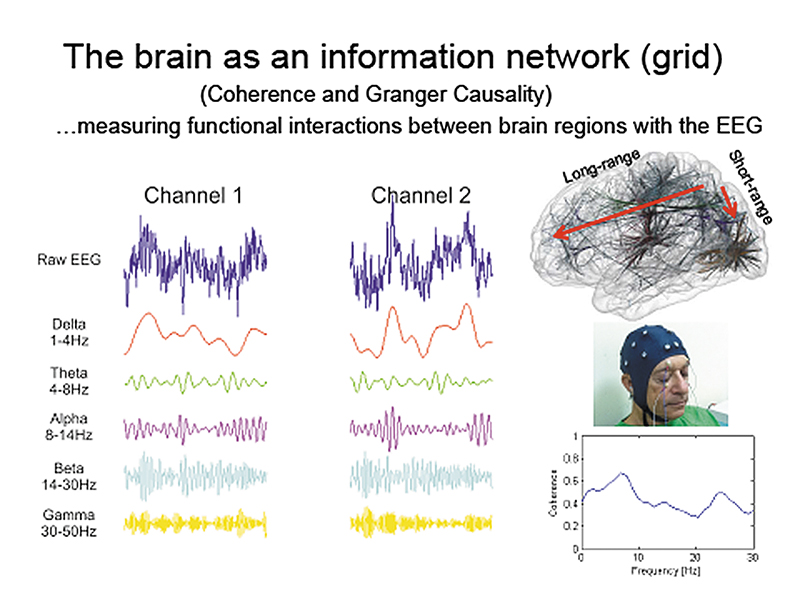
Слайд 3. Электроэнцефалография, позволяющая выявить синхронизирование волн в коре головного мозга и взаимосвязь работы в нем разных центров
Если сравнить пациентов с глаукомой и группу контроля (здоровые лица) и проанализировать волны, идущие в коре головного мозга в обеих группах, то оказывается, что здоровые лица отличаются от больных глаукомой именно характером альфа-2-волн.






