Что касается важности такого параметра, как аксиальная разрешающая способность, на данный момент среднее значение — 5 микрометров — позволяет детектировать самые ранние проявления истончений слоев сетчатки. Самый лучший показатель коммерчески доступного СОКТ — 3 микрометра — позволяет распознавать до 10 слоев сетчатки. Также трехмикронное разрешение значительно улучшает качество визуализации мелких капилляров в режиме ОКТ-ангиографии. Для улучшения качества визуализации, помимо улучшения качества элементов оптической системы, физических характеристик источника излучения и детектора (в технологии СОКТ именно детектор является самым инертным модулем во всем алгоритме обработки), применяют постобработку.
Самый распространенный и простой способ улучшить качество визуализации — сделать многократное сканирование одной и той же локализации структуры. Обработка большого числа сканирований дает возможность убрать цифровой «шум» (стекловидное тело и хориоидея будут отображаться более детально), сделать плавными (естественными) границы оптических слоев (рис. 7). Идея обработки последовательно сделанных сканирований одинаковой локации стали основой технологии ОКТ-ангиографии, которая будет описана далее.
Необходимо упомянуть все промежуточные программные решения, которые имеют непосредственное отношение к алгоритму послойной визуализации сосудистых сплетений. Первое из них — визуализация в режиме En-face.
До появления этого режима визуализации, 3D-структуры представлялись в виде куба (рис. 8) с 3 осями сечений (совпадающих с 3 математическими осями координат).
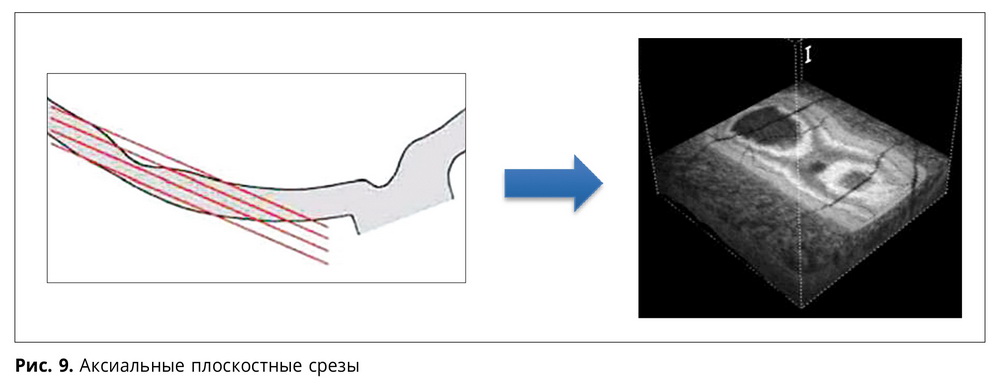
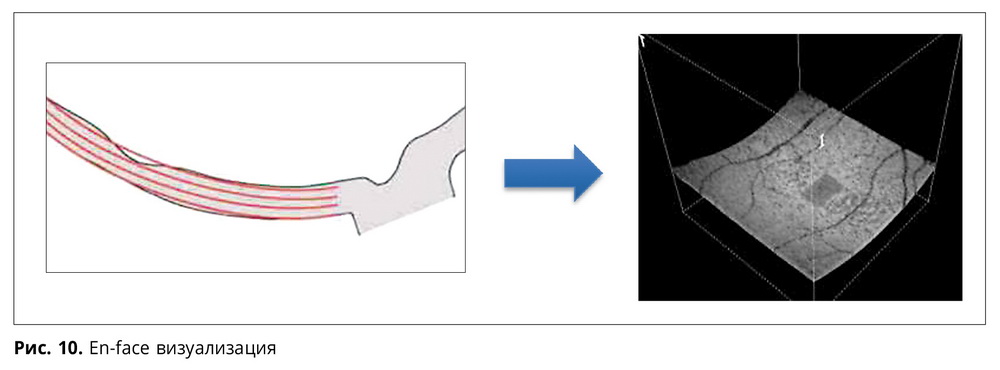
Если плоскостные срезы по ходу луча сканирования имеют диагностический смысл и применяются в практике, то плоскостные срезы перпендикулярно лучу не содержат существенной полезной информации (рис. 9). Идея привязать аксиальное сечение к профилю одного из слоев сетчатки породила режим визуализации оптической плотности заданной области сетчатки (рис. 10).
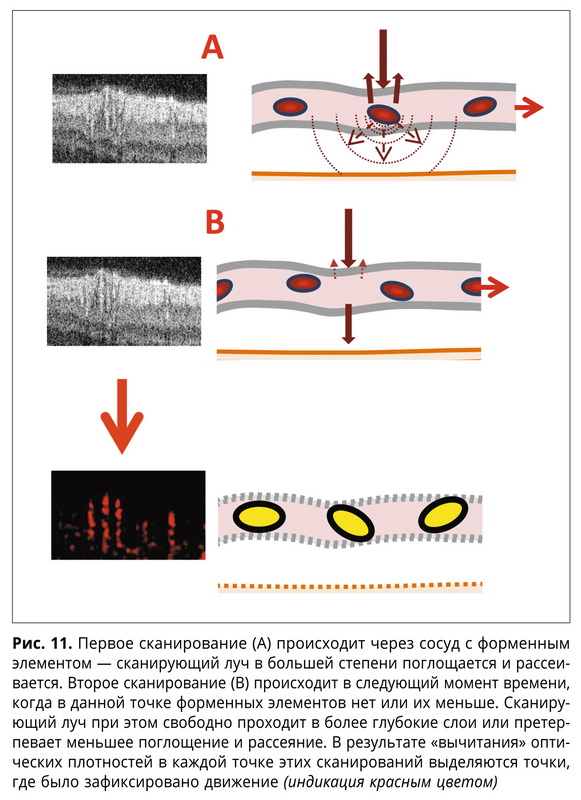
Визуализация сосудистых сплетений стала возможна после объединения технологии сравнения повторных линейных сканирований, En-face и высокой скорости сканирования. Основной принцип обработки основывается на выявлении различных по оптической плотности точек между двумя (или более) последовательными линейными сканированиями. Единственные физиологически обоснованные изменения могут быть в точках движения форменных элементов крови (рис. 11).
Таким образом технология ОКТ-ангиографии может визуализировать только сосуды с кровотоком, причем скорость кровотока имеет определяющее значение. Есть ряд ограничений: не визуализируются сосуды с низкой скоростью кровотока (если сосуд расположен близко к оси сканирования, что в проекции сканирования делает скорость кровотока низкой, несмотря на нормальную скорость сканирования относительно стенок сосуда), вертикальные сосуды (анастомозы).
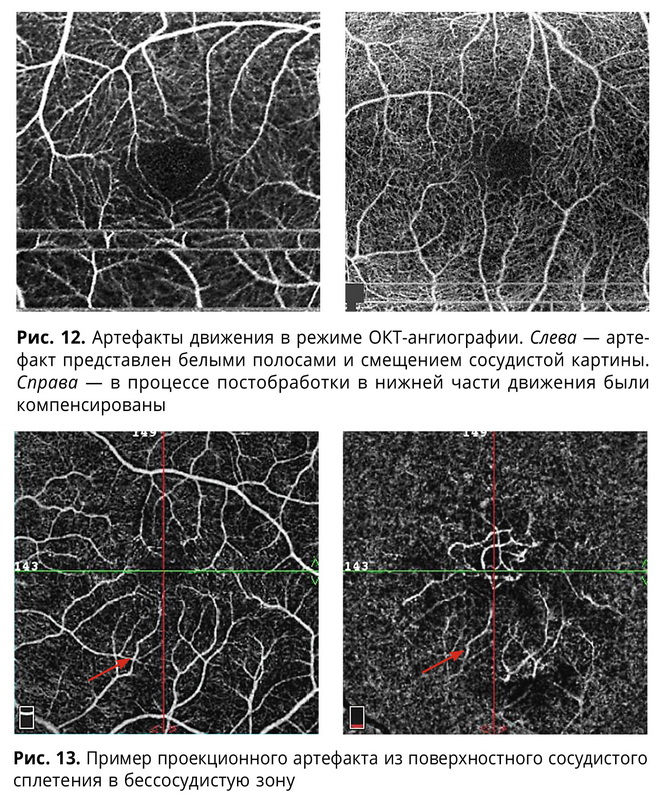
Важной проблемой для технологии ОКТ-ангиографии являются артефакты. К первой группе артефактов можно отнести саккады/движения глаза (рис. 12). Это могут быть как естественные движения глаза, так и движение головы. Отдельную сложность составляет случай непостоянной фиксации.
Для решения данной проблемы разными производителями был предпринят ряд аппаратных и программных мер корректировки движений глаза. Используются как корректировка в режиме реального времени, так и постобработка. Нужно отметить, что увеличение скорости сканирования (что равноценно уменьшению времени процедуры сканирования) является решением для большинства пациентов. Время сканирования меньше 3 секунд является достаточно комфортным.
Другим аппаратным решением является дополнительное устройство сканирования — сканирующий лазерный офтальмоскоп (SLO). Он производит сканирование поверхности структуры независимо от лазера ОКТ и корректирует зону сканирования в зависимости от совершаемых движений. Привязка контроля движений обычно происходит по картине поверхностных крупных сосудов. Наличие SLO также обеспечивает превосходную визуализацию глазного дна. Альтернативой является реконструкция глазного дна от ОКТ-сканирования, но из-за меньшей скорости сканирования данная визуализация может иметь меньшую разрешающую способность и артефакты сканирования.
Другая группа артефактов является следствием некорректной разметки слоев сетчатки. Так как при визуализации сосудистых сплетений имеется прямая привязка к границам слоев сетчатки, то неправильная обработка на этапе разделения структур по оптической плотности приводит к проекционным артефактам (рис. 13).
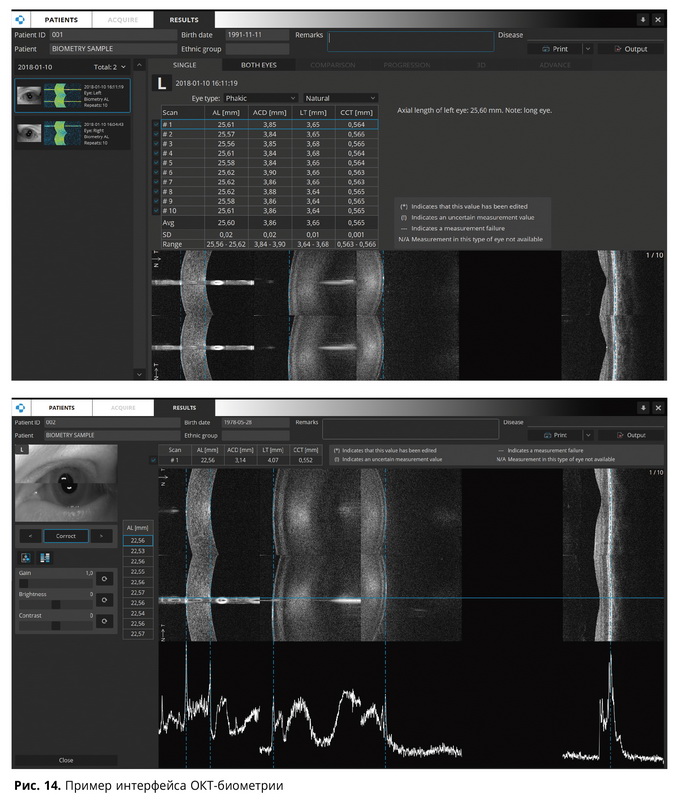
Помимо ОКТ-ангиографии, за последний год были представлены новые области применения технологии ОКТ. Наличие прибора на рынке, который может сканировать передний отрезок глаза и сетчатку без дополнительных адаптеров, позволило создать модуль ОКТ-биометрии (рис. 14).
По точности измерения данный метод превосходит УЗ-аппараты и имеет ряд интересных преимуществ, недоступных в современных оптических биометрах (в том числе биометрах, работающих на принципе SS-ОКТ).
Интересным моментом этого варианта оптической биометрии является сопоставление оптических пиков А-скана со структурной визуализацией. Корректировку границ изменения можно производить относительно структур глаза. Это позволяет исключить любые артефакты, непрозрачные среды и дополнительные структуры (например, контактные линзы).
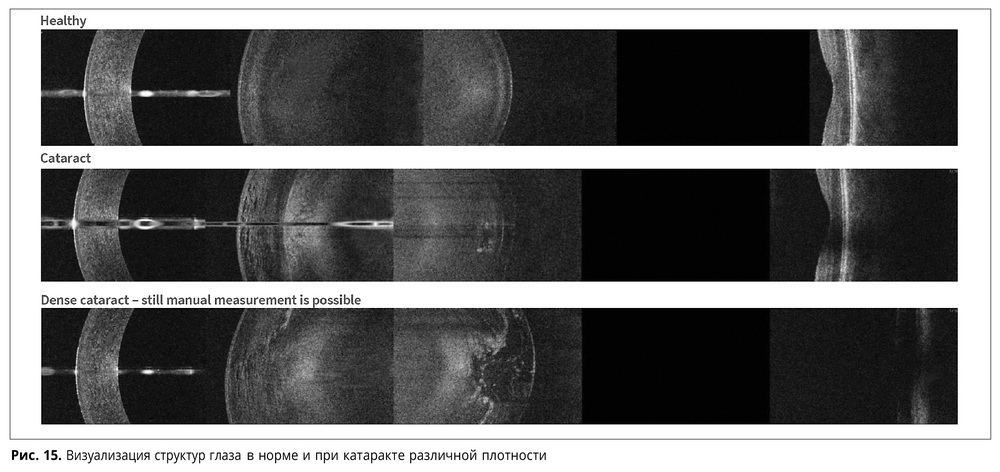
В случае наличия непрозрачных сред различной плотности и раз-личной локализации корректировка оптического пика сетчатки возможна в большем количестве случаев (рис. 15).
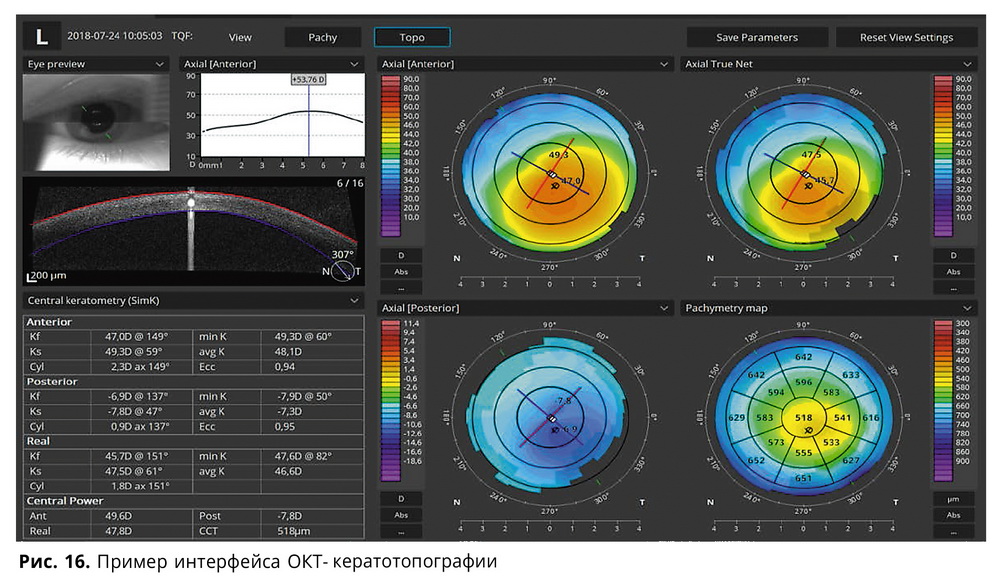
Визуализация переднего отрезка становится более актуальной в разных сферах офтальмологии. Последним нововведением можно назвать ОКТ-кератотопографию (рис. 16). Возможность анализа кривизны поверхности была доступна и раньше (3D-сканирование роговицы дает законченную математическую модель, откуда можно брать данные пахиметрии, толщины эпителия и кривизны передней и задней поверхностей роговицы).
Область применения данных визуализации переднего отрезка очень велика: рефракционная хирургия (данные пахиметрии, толщины эпителия, контроль постоперационных пациентов), контактная коррекция (данные кератотопографии, пахиметрии, биометрии для ортолинз, визуализация слезной пленки под линзой, визуализация посадки линзы, измерение слезного мениска), хирургия глаукомы (визуализация фильтрационной подушки, путей оттока, зоны операции), катарактальная хирургия (визуализация передней и задней капсул хрусталика, ИОЛ, вторичной катаракты), кератопластика и т.д.
Процесс развития направления визуализации с годами лишь ускоряется. Актуальность данного сегмента в офтальмологии невозможно переоценить. Каждый год данная технология находит применение все в больших специализациях. Тандем технических специалистов по разработке ОКТ и медицинских специалистов в области офтальмологии будет все продуктивнее в ближайшем будущем.
Денис Машков
Stormoff group of companies
Страницы: 1 2