В доступной литературе мы не встретили данных о боре в слезе. Поэтому для подтверждения его наличия в пробах была проведена SEM-EDS (сканирующий электронный микроскоп EVO LS 10, Carl Zeiss Group, Германия, и энергодисперсионный рентгеновский спектрометр X-Max 50, Oxford Instruments, Соединенное Королевство) по оригинальной методике.
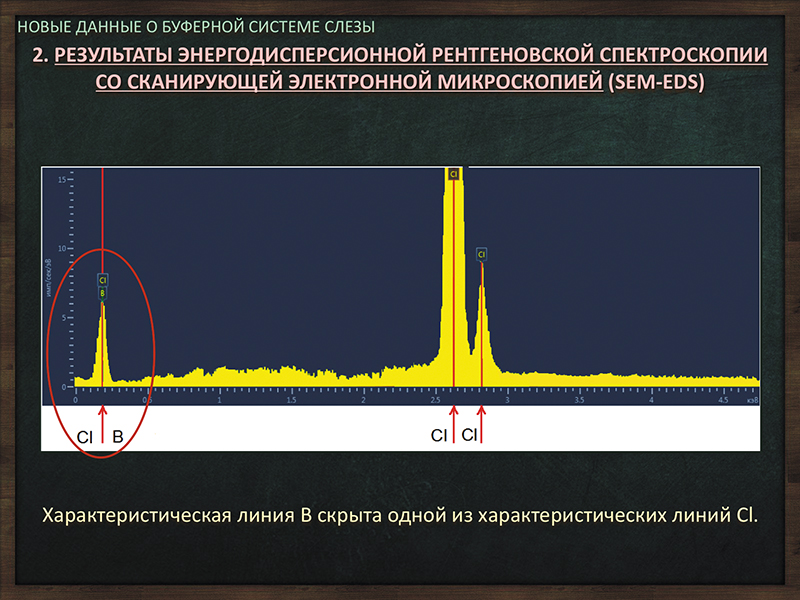
Следует сказать, что о роли бора в организме человека в принципе известно немного. Возможно, это связано с тем, что элементный анализ по бору в биологических средах, в присутствии атомов хлора, представляет отдельную сложную задачу аналитической химии и хемометрии ввиду того, что на получаемых энергодисперсионных спектрах характеристическая линия бора накладывается на одну из характеристических линий хлора (рис. 2, обведено красным).
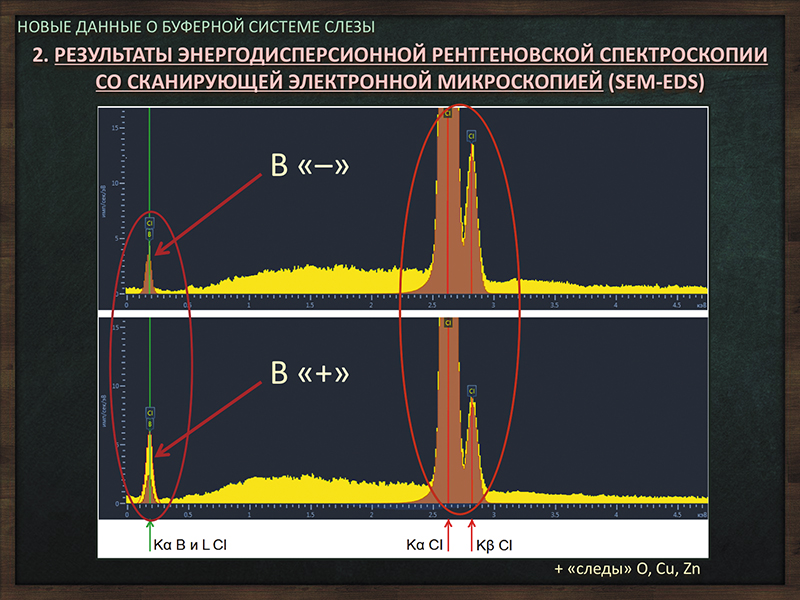
В НИИГБ эта сложная задача по декомпозиции характеристических спектральных линий бора и хлора была решена при помощи компьютерного анализа. Мы проводили математическое моделирование полученных спектров для дифференциального анализа этих химических элементов. Оно позволило на основании достоверно известных линий хлора K Cl и K Cl (рис. 3, обведено красным справа, профили хлора отмечены в коричневом цвете) достраивать теоретический профиль хлора L Cl в проекции возможного профиля бора K B (рис. 3, обведено красным слева, профиль хлора отмечен в коричневом цвете). Так, на верхнем спектре представлены результаты анализа кристаллов, не содержащих бор. Мы видим, что теоретический профиль хлора L Cl полностью перекрывает возможный профиль бора K B (рис. 3, красная стрелка сверху). На нижнем рисунке разность площадей между профилями этих химических элементов (рис. 3, красная стрелка сверху) достоверно свидетельствует о наличии бора в пробах слезы. По данным SEM-EDS в слезе среди ее минеральных компонентов также были выявлены «следовые концентрации» кислорода, меди и цинка.
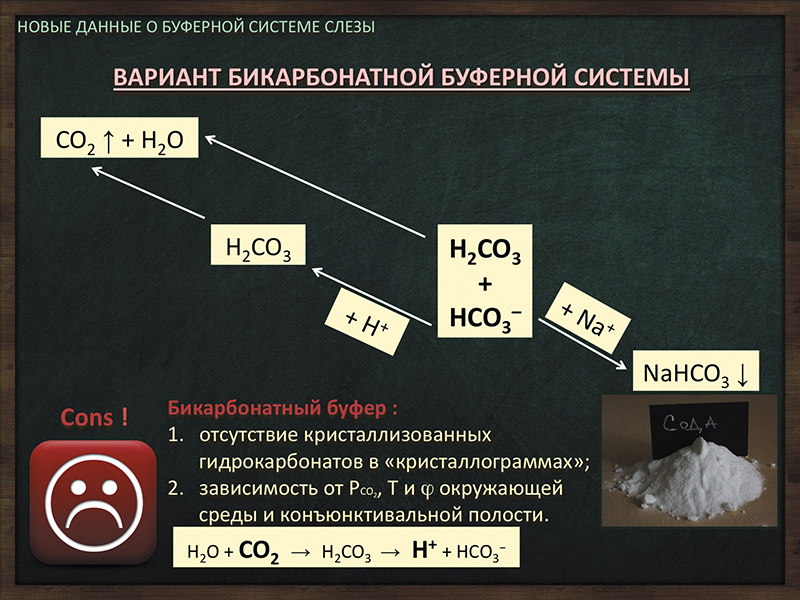
Итак, в свете полученных нами результатов минерального анализа слезы рассмотрим предполагаемый вариант бикарбонатной буферной системы (рис. 4). Если допустить, что в составе слезы была растворенная угольная кислота, то при эвапорации проб она разлагалась бы на углекислый газ и воду. Поэтому в лиофилизатах слезы кристаллов угольной кислоты мы не обнаружили. Если же допустить, что в слезе были растворенные гидрокарбонат-анионы, то при эвапорации они должны были бы кристаллизоваться с образованием солей — гидрокарбонатов натрия или калия. Однако в лиофилизатах слезы кристаллизованных гидрокарбонатов мы не обнаружили. Следовательно, гидрокарбонат-анионы либо вовсе отсутствуют в качестве составляющей бикарбонатного буфера, а значит, отсутствует и сам бикарбонатный буфер как таковой; либо при выпаривании гидрокарбонат-анионы забирают на себя все возможные протоны водорода из биологической среды и образуют угольную кислоту с последующим ее разложением до углекислого газа и воды. Причем последнее означает, что содержание углекислого газа и гидрокарбонатов в слезе непрерывно меняется в зависимости от парциального давления углекислого газа, температуры и влажности окружающей среды и конъюнктивальной полости, что делает предполагаемый бикарбонатный буфер очень «уязвимым».