Главной особенностью хирургии ЗПК, как подчеркивают все исследователи, считается отказ от оводнения хрусталиковых масс перед разрушением ядра для создания его мобильности. Стандартная подготовка к факоэмульсификации включает гидродиссекцию (введение жидкости между задней капсулой и кортикальным слоем) и гидроделинеацию (введение жидкости между ядром и эпинуклеусом) для большей мобильности содержимого хрусталиковой сумки. Возможность гидроделинеации при ЗПК обсуждается, так как она выполняется только вокруг ядра хрусталика для выделения эпинуклеуса, при этом эпинуклеус не отделяется от капсулы и создает механическую «прокладку» для защиты задней капсулы. Некоторые авторы подчеркивают, что при проведении гидроделинеации при ЗПК необходимо исключать риск дополнительной незапланированной гидродиссекции для профилактики проникновения ирригационной жидкости под заднюю капсулу (18,19).
В дополнение к гидроделинеации описан вариант частичной гидродиссекции с минимальным введением жидкости в нескольких квадрантах, так чтобы поток жидкости не распространялся по всей задней капсуле. Однако гарантировать локально ограниченное введение жидкости, особенно при плотных ядрах, сложно, поэтому есть риск незапланированного проникновения в субкапсулярное пространство и необоснованной гидродиссекции.
Собственная техника, безусловно, учитывала предыдущие рекомендации, тем не менее была разработана с учетом ключевой особенности всех этапов операции и исходных анатомических взаимоотношений. А именно: наибольший стресс капсульный мешок испытывает в момент гидродиссекции и гидроделинеации, когда в ограниченном пространстве вводимая под давлением жидкость «препарирует» слои хрусталикового вещества и стремится найти выход. Прочная стандартная задняя капсула и адекватный край капсулорексиса практически всегда выдерживают данную манипуляцию оводнения и выделения ядра, которую справедливо считают основной для создания подвижности ядра и «легкой» факоэмульсификации в последующем.
При задней полярной катаракте существует патологическая адгезия задней капсулы к заднеполярному субкапсулярному помутнению хрусталика, что объясняет высокий риск разрыва капсульного мешка при интенсивных попытках их разделить. Возможно дополнительное локальное ослабление прочности задней капсулы в зоне аномального развития. В итоге при заднеполярной катаракте было решено отказаться от этапа активной гидродиссекции/гидроделинеации с помощью канюли как наиболее рискованного для разрыва задней капсулы.
Все вышеперечисленное привело к тому, что на этапе разрушения ядра заднюю капсулу удалось сохранить и адекватно провести собственно факоэмульсификацию. Имевшие место 2 осложнения из 26 операций произошли на следующем после эмульсификации ядра этапе ‒ аспирации хрусталиковых масс, возможно из-за излишне активного контакта металлических аспирационных/ирригационных наконечников с капсулой.
Выбор вискоэластика с учетом этапа факоэмульсификации имеет важное значение, а в условиях ЗПК приобретает принципиальный характер. В целях сохранения минимальной подвижности иридо-хрусталиковой диафрагмы на всех этапах операции с использованием ирригационного потока жидкости предпочтение отдается дисперсному вискоэластику, который позволяет лучше поддерживать п/камеру, так как он вымывается с определенным трудом. Возможно использование комбинированных вискоэластиков, однако их вымывание происходит быстрее за счет активации «свойства текучести», и стабильность п/камеры становится в результате хуже. Возможно также во время факоэмульсификации ЗПК дополнительно вводить дисперсный вискоэластик, например, в момент извлечения факонаконечника и ирригационных инструментов для поддержания адекватного давления в передней камере (рис. 2).
При имплантации ИОЛ традиционно применяется когезивный вискоэластик для создания безопасного для манипуляций пространства. Он легче удаляется простой ирригацией, часто единым объемным куском, и несмотря на то что измельчение передней камеры на данном этапе возможно, оно менее опасно, чем во время эмульсификации ядра и удаления эпинуклеуса. Может быть полезен прием поэтапного оводнения паразентезов, когда аспирационный наконечник выводится, и данный парацентез оводняется, а ирригационный наконечник остается в глазу для поддержания тонуса.
Работа факоиглой проводилась по следующему сценарию: изначально удалялся верхний эпинуклеарный слой до ядра. Совмещение в наконечнике трех действий с этапным включением каждого в последовательности ‒ ирригация, аспирация, эмульсификация ‒ позволяет на этапе разрушения ядра проводить локальную гидроделинеацию (ирригацию) до того момента, когда наконечник погружается в вещество хрусталика (ирригация+аспирация+эмульсификация), но предупреждает незапланированную опасную гидродиссекцию.
Затем с учетом плотности ядра проводилась вакуумная фиксация ядра (ирригация+аспирация), далее разлом его центральной части, причем полученные два фрагмента-половинки ядра минимально «разводились» в стороны для профилактики стресса задней капсулы. Далее ядро не вращалось, проводили еще один разлом ядра рядом для получения свободного сегмента, который эмульсифицировался.
Таким образом, этапным формированием «узких» сегментов за счет изменения «угла атаки» наконечника удавалось удалить ядро в нижнем сегменте капсульного мешка (практически от 4 до 8 часов). Свободное от ядра пространство играет положительную роль в профилактике разрыва задней капсулы, так как препятствует патологическому повышению гидродинамического давления внутри капсульного мешка. Дальнейшие манипуляции становятся более безопасными, наличие эпинуклеуса под оставшимся фрагментом ядра позволяет проводить минимальное этапное вращение ядра вокруг своей оси для продолжения разлома и удаления сегментов. Данная техника (но с вариантом активного оводнения хрусталика) описана ранее как «сегментарный разлом ядра» и по сути является вариантом техники step-by-step, chop in situ (20, 21).
Важное значение имеет баланс ирригации и аспирации, для достижения которого используются предустановки аспирации – уровень включения вакуума аспирации не с нулевого положения (начиная с 30 mmHg) для быстрого отклика на ирригационный поток (высота бутылки не более 70 мм). Больший (80 мм и более) и меньший (60 мм и меньше) ирригационный поток может спровоцировать нестабильность передней и задней камер глаза и как следствие колебания задней капсулы хрусталика. Максимальный уровень вакуума в соответствии с установленным уровнем ирригации рекомендуется не более 250 mmHg. Предпочтение отдается линейному контролю вакуума для «управляемой» реакции хирурга на процесс аспирации. В то же время поток аспирации предпочтительнее оставить фиксированным для создания исходного стабильного уровня гидродинамики (не более 30 cc/min). При линейном контроле потока и вакуума вполне вероятно запаздывание ответа на ситуацию, при фиксированном потоке и вакууме возможна менее управляемая реакция, при необходимости следует уменьшить воздействие.
Мощность ультразвука определяется плотностью ядра и должна быть достаточной для его разрушения, однако в случае ЗПК на этапе разлома чаще уменьшается (на 20-30%) для профилактики несанкционированного удаления эпинуклеуса под ядром. Последний выполняет защитную функцию в момент разрушения ядра, ограничивая механические воздействия на опасную зону задней капсулы. На этапе факоразлома УЗ наконечник должен обеспечить роль вакуумного пинцета для последовательного сегментарного разделения ядра. Выбор режима УЗ – торсионный постоянный. Торсионные движения факоиглы исключают колебательные, «от иглы ‒ к игле», движения ядра, которые характерны для продольного ультразвука в момент внедрения. Также в отличие от пульсового режима непрерывный режим ультразвука меньше «отталкивает» фрагменты ядра от факоиглы. При удалении полученных фрагментов мощность УЗ по необходимости может быть увеличена. Данные рекомендации относятся к использованному в работе прибору – «Infinity» (Alcon).
При мягком ядре и несостоятельных попытках факоразлома продолжалось послойное удаление ядра до «безопасной глубины» ‒ из собственного опыта несколько больше половины толщины хрусталика. Понятие «безопасная глубина» не вполне четкое определение, поэтому в практике применяется следующий подход. Как правило, при мягком ядре нет четкого разграничения на собственно ядро и эпинуклеус, поэтому постепенное, с ограничением мощности УЗ, удаление ядерного слоя плавно переходит в удаление эпинуклеарного слоя. При такой технике ирригационные потоки в основном циркулируют в передней камере, а также пассивно попадают и накапливаются в хрусталиковом веществе, постепенно отделяя эпинуклеус от задней капсулы. Отсутствие активного принудительного оводнения (как при гидродиссекции канюлей) не увеличивает внутрикапсулярное давление и не увеличивает стресс задней капсулы. Таким образом, процесс эмульсификации ядра подготавливает следующий этап операции.
Следующий важный этап факоэмульсификации при ЗПК – удаление эпинуклеуса. Даже с учетом неполной подготовки ядра к эмульсификации ввиду отказа от полноценного оводнения, манипуляции с целым ядром и его фрагментами проводятся вдали от задней капсулы с защитным слоем в виде эпинуклеуса. Момент освобождения эпинуклеуса от задней капсулы в отсутствие предварительной гидродиссекции, на первый взгляд, – самый опасный момент. С другой стороны, существуют рекомендации как раз в этот момент проводить дополнительную гидродиссекцию, которую можно считать более безопасной, так как капсульная сумка практически свободна и риск повышения внутрикапсульного давления минимален.
Однако рекомендация дополнительной активной гидродиссекции эпинуклеуса представляется неочевидной, так как риск «быстрого» мало предсказуемого разделения субкапсулярного помутнения и собственно капсулы сохраняется. Удаление эпинуклеуса может проводиться факонаконечником (аспирация + минимальный уровень ультразвука) или аспирационно-ирригационным наконечником. В собственной практике выбор способа зависит от плотности эпинуклеуса. При плотном эпинуклеусе предпочтение отдается аспирации факонаконечником, при мягком ‒ используется раздельная бимануальная аспирационно-ирригационная техника. В процессе, предшествующем эмульсификации ядра и последующего удаления эпинуклеуса, происходит «медленная» пассивная гидродиссекция, так как «комфортный» ирригационный поток поддерживает глубину передней/задней камеры и одновременно позволяет деликатно отделять слой эпинуклеуса от капсулы. Сам эпинуклеус фиксируется за визуально свободный край аспирационным наконечником, последовательно отделяется от капсулы и аспирируется.
В итоге после удаления эпинуклеуса чаще всего наблюдается «ложное отверстие» – округлая зона задней капсулы в центре, которая соответствует области максимального контакта заднеполярного помутнения с капсулой. Вокруг располагается зона периферических отделов капсулы с остаточными субкапсулярными хрусталиковыми массами. Разительный контраст между двумя зонами визуально имитирует дефект задней капсулы (рис. 2). В отличие от центрального помутнения периферические хрусталиковые массы рыхло прилежат к задней капсуле и удаляются стандартной техникой по направлению от периферии капсульного мешка к его центру. Разделение ирригации и аспирации в бимануальной технике потенциально лучше обеспечивает стабильность передней камеры (рис. 2).
Собственный опыт факоэмульсификации ЗПК показал эффективность приемов профилактики разрыва задней капсулы, предупреждающих повышение давления в капсульном мешке и колебаний иридо-капсулярной диафрагмы. На подготовительном этапе, этапе факоэмульсификации и удалении эпинуклеуса осложнений не произошло. Два случая разрыва задней капсулы произошли на этапе аспирации ‒ полировки задней капсулы. Каких-либо отличительных особенностей до операции и во время данных осложненных операций не отмечено, разрыв задней капсулы может быть объяснен контактом аспирационных/ирригационных наконечников с зоной наибольшего истончения. Исходя из этого, безопасность полировки задней капсулы при ЗПК признана сомнительной, поэтому в собственной практике больше не применяется. Предпочтения в раздельной бимануальной технике ирригации/аспирации обоснованы в более прогнозируемой глубине передней камеры, в том числе и при извлечении наконечников, которые можно проводить раздельно.
Внедрение фемтоассоциированной технологии факоэмульсификации открыло новые перспективы хирургии ЗПК. В первую очередь, это относится к возможности фемтоделинеации взамен гидроделинеации, что облегчает разделение ядра и эпинуклеуса по слоям без резкого повышения давления внутри капсульного мешка. Вместе с тем, дискуссия о преимуществах фемтотехнологии при ЗПК продолжается, так как случаи разрыва задней капсулы описаны и при этой технологии (22-24).
Далее, имплантация ИОЛ в капсульный мешок и все последующие этапы проходили без особенностей, вместе с тем с соблюдением дополнительной осторожности (рис. 2). В итоге 24 операции прошли без осложнений, в 2 случаях произошел разрыв задней капсулы на этапе аспирации хрусталиковых масс, механизм осложнения связан с избыточно активными попытками очистить заднюю капсулу в момент механической полировки аспирационной канюлей. Удаление остатков хрусталиковых масс в данных случаях проведено в среде вискоэластика канюлей Simcoe; выполнена имплантация гидрофобной моноблочной заднекамерной ИОЛ на переднюю капсулу в цилиарную борозду с ущемлением оптики в сохранном «окне» переднего капсулорексиса. Наблюдение в течение 2 лет показало стабильное положение ИОЛ со смешанной фиксацией и отсутствие дополнительных осложнений (рис. 5).
 |
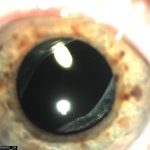 |
| Рис. 5. Артифакия. ИОЛ со смешанной фиксацией, оптика «ущемлена» в переднем капсулорексисе. Правильное центральное положение. МКОЗ=0,4 (причина неполной МКОЗ — неоваскулярная форма ВМД). | |
Заключение
Полученные функциональные результаты еще раз свидетельствуют о возможности успешной факоэмульсификации с минимальной частотой осложнений у пациентов с ЗПК. Известные хирургические приемы, направленные на снижение колебаний давления как в капсульном мешке так в передней камере в целом, были использованы в данной практике.
Основные особенности предлагаемой техники операции заключаются:
— для стабильного положения передней/задней камеры введение растворов и капулорексис проводятся через парацентезы до формирования основного разреза
— полный отказ не только от гидродиссекции, но и от гидроделинеации на этапе подготовки к эмульсификации собственно ядра, также отказ от дополнительной гидродиссекции остаточного эпинуклеуса перед его аспирацией
— выбор режима постоянного торсионного ультразвука для уменьшения колебательных движений фрагментов ядра
— уменьшение параметров гидродинамики (в качестве ориентира – высота бутылки для ирригации не более 70 мм, аспирация не более 30 cc/min, вакуум не более 250 mmHg на приборе «Infinity»)
— техника последовательного сегментарного пошагового разлома ядра во время эмульсификации с минимальным вращением фрагментов при снижении мощности УЗ (до 30%)
— выбор раздельной бимануальной техники ирригации/аспирации для более прогнозируемой глубины передней камеры, в том числе и при извлечении наконечников, которые можно проводить раздельно.
— отказ от полировки задней капсулы для профилактики механического контакта и повреждения задней капсулы.
Литература
- R.Vasavada, V.A.Vasavada Managing the posterior polar cataract: An update 2017 Indian J Ophyhalmol Dec; 65 (12): 1350–1358.
- Nagappa S, Das S, Kurian M, Braganza A, Shetty R, Shetty B, et al. Modified technique for epinucleus removal in posterior polar cataract. Ophthalmic Surg Lasers Imaging. 2011;42:78–80.
- Lee MW, Lee YC. Phacoemulsification of posterior polar cataracts – A surgical challenge. Br J Ophthalmol. 2003;87:1426–7.
- Allen D, Wood C. Minimizing risk to the capsule during surgery for posterior polar cataract. J Cataract Refract Surg. 2002;28:742–4.
- Lee MW, Lee YC. Phacoemulsification of posterior polar cataracts – A surgical challenge. Br J Ophthalmol. 2003;87:1426–7.
- Vasavada AR, Singh R. Phacoemulsification with posterior polar cataract. J Cataract Refract Surg. 1999;25:238–45.
- Osher RH, Yu BC, Koch DD. Posterior polar cataracts: A predisposition to intraoperative posterior capsular rupture. J Cataract Refract Surg. 1990;16:157–62.
- Иошин И.Э. Амбулаторная хирургия катаракты. М.Апрель- 2016.
- Siatiri H, Moghimi S. Posterior polar cataract: Minimizing risk of posterior capsule rupture. Eye (Lond) 2006;20:814–6.
- Anis AY. Understanding hydrodelineation: The term and the procedure. Doc Ophthalmol. 1994;87:123–37.
- Masket S. Consultation section. J Cataract Refract Surg. 1997;23:819–82.
- Нayashi K, Hayashi H, Nakao F, Hayashi F. Outcomes of surgery for posterior polar cataract. J Cataract Refract Surg. 2003;29:45–9.
- Fine IH, Packer M, Hoffman RS. Management of posterior polar cataract. J Cataract Refract Surg. 2003;29:16–9.
- Das S, Khanna R, Mohiuddin SM, Ramamurthy B. Surgical and visual outcomes for posterior polar cataract. Br J Ophthalmol. 2008;92:1476–8.
- Kumar S, Ram J, Sukhija J, Severia S. Phacoemulsification in posterior polar cataract: Does size of lens opacity affect surgical outcome? Clin Exp Ophthalmol. 2010;38:857–61.
- Kymionis GD, Diakonis VF, Liakopoulos DA, Tsoulnaras KI, Klados NE, Pallikaris IG, et al. Anterior segment optical coherence tomography for demonstrating posterior capsular rent in posterior polar cataract. Clin Ophthalmol. 2014;8:215–7.
- Тitiyal JS, Kaur M, Falera R. Intraoperative optical coherence tomography in anterior segment surgeries. Indian J Ophthalmol. 2017;65:116–21.
- Vasavada AR, Raj SM. Inside-out delineation. J Cataract Refract Surg. 2004;30:1167–9.
- A, Aravind S, Vadi K, Natchiar G. Bimanual microphaco for posterior polar cataracts. J Cataract Refract Surg. 2006;32:914–7.
- Vasavada A, Singh R. Step-by-step chop in situand separation of very dense cataracts. J Cataract Refract Surg. 1998;24:156–9.
- Иошин И.Э. Факоэмульсификация. М.Апрель- 2014.
- Vasavada AR, Vasavada V, Vasavada S, Srivastava S, Vasavada V, Raj S, et al. Femtodelineation to enhance safety in posterior polar cataracts. J Cataract Refract Surg. 2015;41:702–7.
- Titiyal JS, Kaur M, Sharma N. Femtosecond laser-assisted cataract surgery technique to enhance safety in posterior polar cataract. J Refract Surg. 2015;31:826–8.
- Alder BD, Donaldson KE. Comparison of 2 techniques for managing posterior polar cataracts: Traditional phacoemulsification versus femtosecond laser-assisted cataract surgery. J Cataract Refract Surg. 2014;40:2148–51.
Страницы: 1 2






