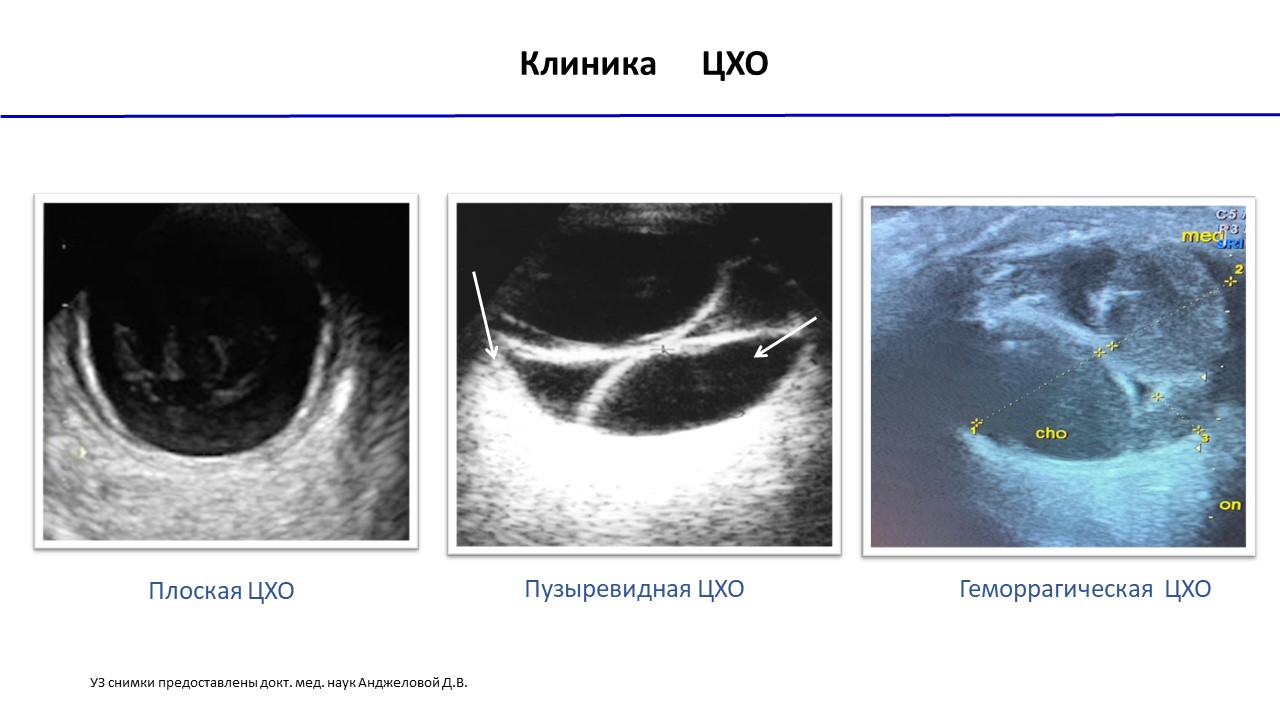
Цилихориоидальная отслойка (ЦХО) – наиболее часто встречающееся осложнение, которое подразделяется на серозную, геморрагическую, экссудативную. Клиника ЦХО сопровождается ухудшением зрительных функций (снижение остроты зрения, сужение поля зрения, изменение рефракции), цилиарной болезненностью, изменением гидростатики (уменьшение глубины передней камеры, сдвиг кпереди иридохрусталиковой диафрагмы). Признаками ЦХО являются мелкая передняя камера, складки сосудистой оболочки, отслойка сосудистой оболочки, что подтверждается УЗИ (рис. 1). Как правило, ЦХО начинается с отслойки цилиарного тела, и при проведении оперативных терапевтических мероприятий оболочки прилегают, и процесс благополучно завершается. Более сложная ситуация возникает при геморрагической ЦХО.
Профессор В.П. Еричев обратил внимание, что при ЦХО может страдать роговица по причине низкого ВГД, при этом возникает складчатый кератит, требующий принятия своевременных и энергичных мер; в противном случае может возникнуть вторичная дистрофия роговицы.
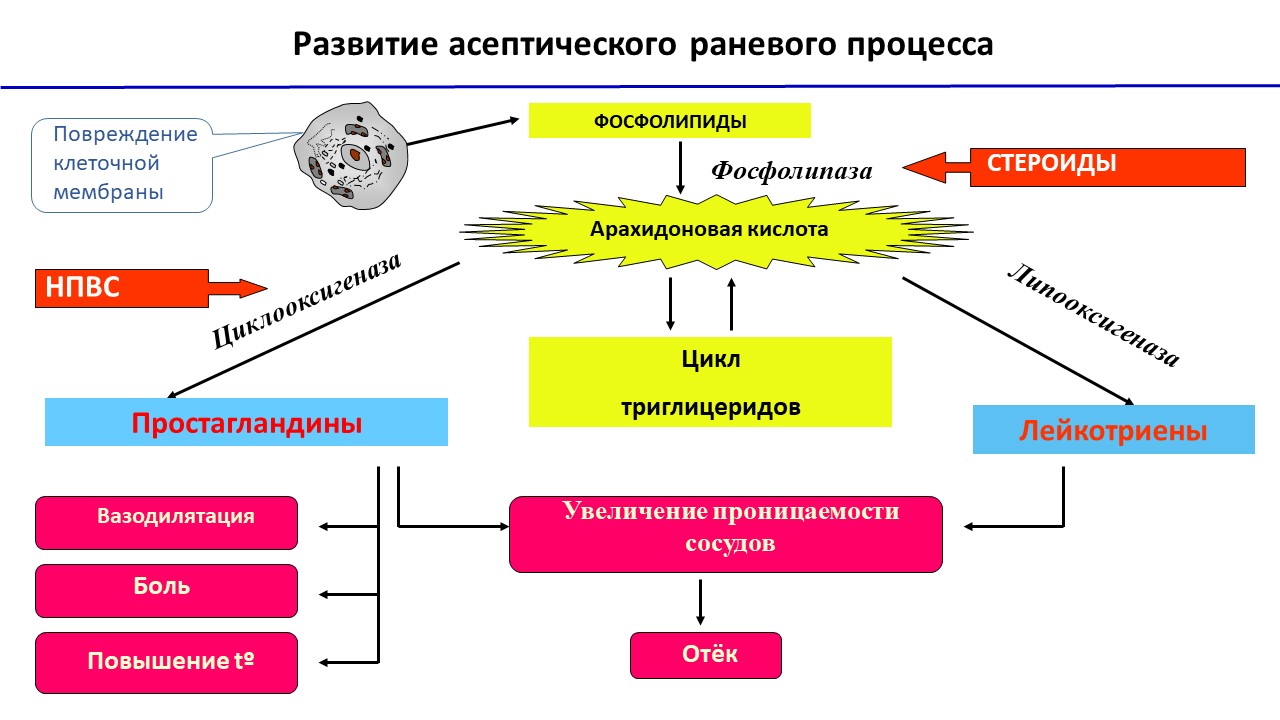
Любое хирургическое вмешательство сопровождается повреждением ткани, связанного с развитием асептического раневого процесса, схема которого представлена на рис. 2. Повреждение ткани приводит к нарушению целостности клетки; фрагменты липидного слоя клетки взаимодействуют с ферментом фосфолипазы, следствием чего является появление арахидоновой кислоты; при взаимодействии таких ферментов, как циклооксигеназа и липоокигеназа, запускается цикл триглицеридов, который заканчивается образованием простагландинов и лейкотриенов, которые определяют сущность патофизиологического асептического воспаления. Этот процесс может быть прерван применением НПВС или кортикостероидов.
Клиника асептического воспаления может представлять собой перекорнеальную инъекцию, ирит, появление фибрина во влаге передней камеры, приводящее в некоторых случаях к возникновению асептического гипопиона; появление фибрина может также вызвать бомбаж радужки. Эти состояния требуют энергичного применения противовоспалительной терапии.
Асептическое воспаление, вызванное применением препаратов, содержащих бензалкония хлорид, может привести к образованию рубцовой блокады в зоне хирургического вмешательства, между конъюнктивой с склерой, что препятствует оттоку ВГЖ. В таких случаях необходимо использовать НПВС, имеющие выраженный терапевтический, анальгезирующий эффект, способствующие ингибированию миоза, что важно при лечении ирита или иридоциклита.
Для получения медикаментозного мидриаза, по мнению докладчика, следует использовать препараты, обладающие циклоплегическими свойствами; чаще применяют комбинированные препараты.
Нередким осложнением АГО являются геморрагические осложнения: гифемы (появление крови во влаге передней камеры), гемофтальм (появление крови в стекловидном теле), экспульсивная геморрагия.
Наружная фильтрация может возникнуть в первые часы или дни после проведения АГО. Причиной возникновения часто служит недостаточная герметизация или неправильно наложенный шов. В более поздние сроки причиной могут служить аваскулярные, кистозные, тонкостенные фильтрационные подушки, провоцирующие наружную фильтрацию, опасную вероятностью возникновения вторичного инфицирования. Такое состояние фильтрационных подушек может быть следствием применения цитостатических препаратов.
Офтальмогипертензия, как осложнение АГО, может возникать как в ранние, так и в поздние сроки (чаще). Асептическое воспаление, приводящее к конъюнктивально-склеральной или склеро-склеральной блокаде в зоне хирургического вмешательства и, как следствие, к повышению ВГД, часто является следствием применения топических препаратов, содержащих консерванты.
Рубцевание в зоне хирургического вмешательства может возникнуть на ранней стадии после операции (рис. 3-1); чаще возникают кистозные подушки (рис. 3-2), свидетельствующие о недостаточном оттоке ВГЖ. Такие кистозные подушки являются показанием для проведения нидлинга (рис. 3-3,4).
Тяжелым осложнением АГО является «злокачественная» глаукома. Частота встречаемости 1,6-2,1%; причины: блокада оттока ВГЖ через pars plicata цилиарного тела с обратным ее оттоком в стекловидное тело; признаки: мелкая передняя камера, закрытый угол передней камеры, высокий уровень ВГД, отсутствие фильтрационной подушки, отрицательная проба Зайделя, дополнительные полости в стекловидном теле (УЗИ).
Лечение: 1 этап – инстилляции мидриатиков для достижения циклоплегии; топические препараты для снижения продукции ВГЖ; осмотерапия. Важно: исключить миотики и аналоги простагландинов. 2 этап – иридэктомия, разрушение гиалоидной мембраны для устранения цилиарного блока. 3 этап – витрэктомия через pars plana лучше с аспирацией жидкости из дополнительных полостей; витреоленсэктомия.
Постоперационные эндофтальмиты не часты, но их угроза для зрения – велика. Эндофтальмиты связаны с возникновением инфекции, вызванные нарушением целостности фильтрационной подушки. Для клиники характерно появление гипопиона. Важное значение имеет своевременное начало противобактериальной терапии, применяется витрэктомия.
Антибиотики должны обладать следующими свойствами: бактерицидное действие, высокая проникающая способность, широкий спектр действия, хорошая переносимость, низкая резистентность микроорганизмов к препарату. Автор обратил внимание на фторхинолоны 4 поколения.
С докладом на тему «Практические аспекты анти-VEGF терапии возрастной макулярной дегенерации» выступила к.м.н. А.А. Плюхова. В соответствии с классификацией, используемой в Британских клинических рекомендациях, ВМД подразделяется на раннюю (с низким риском прогрессирования – при наличии небольшого количества друз, средним риском прогрессирования – при наличии сливных друз, высоким риском прогрессирования – при наличии ретикулярных друз, друзеноидной отслойки), позднюю ВМД (промежуточную), позднюю ВМД (сухая или атрофическая форма), позднюю ВМД (влажная активная, экссудативная или неваскулярная форма), позднюю ВМД (влажная неактивная форма – наличие субретинального фиброза).
В диагностике широкое применение приобрела ОКТ: определение высоты и площади макулярного отека; определение структурных характеристик отека (кистозные изменения, отслойка нейроэпителия); выявление наличия витреоретинальных тракций; выявление наличия эпиретинального фиброза; определение положения задней гиалоидной мембраны стекловидного тела; наблюдение за эффективностью лечения макулярного отека.
Общепринятыми факторами риска прогрессирования ВМД являются наличие экссудативной формы ВМД на парном глазу; крупные (особенно мягкие) друзы, связанные с ВМД; изменения в РПЭ; изменение друз (рост, увеличение площади и объема, генетические маркеры). На рис. 1 представлены признаки активности заболевания: наличие СРЖ является признаком благоприятного прогноза; ИРЖ – признак худших функциональных результатов; наличие жидкости под ретинальным пигментным эпителием ассоциируется с низкой ОЗ.
При неваскулярной форме ВМД показан значительный терапевтический эффект после ИВВ анти-VEGF препаратов. Существует три основных подхода лечения и увеличения интервала между ИВИ. Реактивный фиксированный режим: данный способ характеризуется подбором максимального фиксированного интервала лечения на основании оценки активности заболевания (преимущественно после загрузочной фазы) с возможностью дальнейшего уменьшения. Фиксированный режим: для данного режима характерен регулярный интервал между ИВИ вне зависимости от потребности пациента. Режим Treat@Extend предусматривает постепенное изменение интервала лечения в зависимости от активности заболевания.
К.м.н. А.А. Плюхова отметила, что на практике встречаются случаи недостаточного ответа на анти-VEGF терапию (рис. 2) или стойкой активности заболевания. Речь идет о наличии стойкой экссудации (с учетом дифференцированной оценки изменений в динамике), прогрессирующем фиброзе, неразрешившимся или новом кровоизлиянии. Однако в некоторых случаях будет неправильным говорить о недостаточном ответе на терапию, а именно: после первых 3-5 месяцев лечения, при нерегулярном лечении и неправильно подобранном режиме терапии, при неправильной оценке признаков активности заболевания, при необоснованно завышенных ожиданиях от терапии.
Критерии активности ВМД: анамнестические данные — жалобы на ухудшение зрения, появление пятен перед глазами, искажение линий; визометрия — снижение ОЗ вдаль, трудности при чтении, особенно в условиях пониженной освещенности;офтальмоскопия — субретинальная неоваскуляризация, сопровождающаяся серозной отслойкой нейро- и пигментного эпителия сетчатки, отеком сетчатки и кровоизлияниями; ФАГ – накопление красителя и его ликедж в зоне СНМ; ОКТ – отек, утолщение сетчатки в центре, неровный верхний контур СНМ, элевация сетчатки вокруг СНМ; ОКТ-А – четкая форма СНМ в виде кружева или коралла, ветвящиеся множественные мелкие капилляры, наличие анастомозов и петель, строение терминальных сосудов, указывающее на наличие периферийной аркады.
Автор обратила на важность правильной оценки структурных изменений сетчатки для определения необходимости проведения анти-VEGF терапии. Это – экстравазальный выход флюоресцеина на ФАГ, фиброваскулярная отслойка пигментного эпителия, суб- или интраретинальная жидкость на ОКТ, усиление кровоизлияний. Повреждения сетчатки, симулирующие ликедж на ОКТ, не требующие проведения анти-VEGF терапии: внешние ретинальные тубуляции, хронические интраретинальные кисты.
Далее к.м.н. А.А. Плюхова привела практические советы экспертов – критерии изменения интервала между инъекциями. Увеличение интервала: отсутствие снижения ОЗ ≥ 5 букв, отсутствие жидкости на ОКТ или наличие СРЖ, количество которой не уменьшается при уменьшении интервала между инъекциями и отсутствие предыдущих попыток увеличить интервал. Сохранение интервала: отсутствие снижения ОЗ ≥ 5 букв, отсутствие жидкости на ОКТ или наличие СРЖ, количество которой не уменьшается при уменьшении интервала между инъекциями; предыдущие попытки увеличить интервал между инъекциями привели к реактивации заболевания. Уменьшение интервала: снижение ОЗ ≥ 5 букв или наличие признаков активности заболевания на ОКТ – ИРЖ и/или новые макулярные кровоизлияния и/или нестабильная СРЖ.
С докладом «Оптическая когерентная томография в диагностике меланом хориоидеи» выступила к.м.н. А.С. Стоюхина. Ежегодно меланому хориоидеи (МХ) выявляют у 7-13 человек на 1 000 000 населения, при этом на момент выявления средняя проминенция достигает 4,6-6,3 мм. Локализация МХ: преэкваториально (в т.ч. цилиарное) – 17-23%; область экватора – 26-27%; постэкваториально – 46-57% (62% темпоральная область); билатеральная локализация – до 2%.
Офтальмоскопическая картина МХ: аспидно-серый цвет, поля оранжевого пигмента, вторичная отслойка сетчатки, складчатость сетчатки по периферии опухоли.
Обследование группы пациентов выявило томографические признаки МХ, которые можно использовать в ранней и дифференциальной диагностике МХ (рис. 1). Были обследованы пациентами с маленькими МХ с использованием ОКТ в режиме EDI, т.е. глубокого сканирования, позволяющего детально исследовать состояние хориокапиллярного слоя и в ряде случаев оценить заднюю поверхность хориоидеи. По данным исследования, доказанными ОКТ-признаками МХ являются асимметрия профиля хориоидеи, уплощение по краям «хориоидального комплекса», округлые полости на уровне внутренних слоев «хориоидального комплекса», интенсивно или умеренно гиперрефлективная структура внутренних слоев «хориоидального комплекса», повреждения мембраны Бруха, нарушение дифференцировки слоев сетчатки, признаки инфильтрации наружных слоев сетчатки, отслойка нейроэпителия по скату очага, разрыв фоторецепторов, скопление транссудата.
Сравнение томографии с результатами гистологического исследования показало совпадение по следующим признакам: разрушение мембраны Бруха, наличие гиперрефлективных изменений на уровне РПЭ (пролиферация), изменение фоторецепторов (нарушение целости), наличие отслойки нейроэпителия, наличие интраретинальных полостей.
При анализе томографической картины в зависимости от размеров опухоли, последовательность формирования томографических признаков представлена следующим образом (рис. 2). По мере роста опухоли происходит увеличение толщины меланомы с распространением ее на все слои хориоидеи, а также увеличение оптической плотности в зоне опухоли.
ОКТ-ангиография показала, что собственные сосуды МХ можно выявить при ее толщине в 1,4 мм; при толщине до 1,9 мм в глубоком капиллярном сплетении сетчатки выявляются сосудистые петли; по мере роста опухоли в слое хориокапилляров и слое крупных сосудов хориоидеи – сосудистые петли, являющиеся признаком формирования ретинотуморальных шунтов; при толщине опухоли от 2,93 мм выявляются сами ретинотуморальные шунты.
Автор подчеркнула, что при диагностике МХ необходимо помнить о дистантной макулопатии (ДМ) (рис. 3), представляющей собой экссудативные изменения макулярной зоны, развивающиеся при локализации опухоли вне макулярной зоны. Может быть «гравитационная» при расположении опухоли над макулярной зоной, «тракционная» за счет натяжения сетчатки по краю МХ; может возникнуть за счет нарушения аксоплазматического тока при локализации МХ в юкста- и перипапиллярной зоне; помимо отслойки нейроэпителия характеризуется кистозными изменениями в макулярной зоне. Таким пациентам необходимо проводить детальный осмотр глазного дна по всем меридианам.
Интерес представляет МХ, развившаяся из невуса. Отличительными признаки МХ от невуса по данным ОКТ являются следующие: асимметрия увеличения профиля хориоидеи, округлые полости на уровне внутренних слоев хориоидеи, компрессия хориокапилляров рядом с очагом, ОНЭ по скатам, разрыв фоторецепторов, кисты на вершине очага, гиперрефлективные интраретинальные включения; по данным ОКТ-А: хориокапиллярные петли по краям, единичные атипично расположенные прямолинейные сосуды в наружных слоях хориоидеи.
Меланомы хориоидеи, развившиеся из невуса, толщиной до 2 мм, как правило, характеризуются наличием офтальмоскопически беспигментной зоны и пигментированной зоны. Беспигментная часть: участки деструкции хориокапиллярного слоя, неровности поверхности «хориокапиллярного комплекса», прямые и косвенные признаки нарушения целости мембраны Бруха, зоны скопления умеренно гиперрефлективного субретинального транссудата; пигментированная часть: единичные полости на уровне внутренних слоев хориоидеи, гладкий профиль поверхности «хориоидального комплекса», сохранность мембраны Бруха, участки повреждения РПЭ.
К.м.н. А.С. Стоюхина отметила, что при диагностике МХ по данным ОКТ необходимо обращать внимание на состояние «хориоидального комплекса», а именно: на увеличение проминенции, оптическую плотность зоны интереса, на наличие неровности поверхности «хориоидального комплекса», на возможность визуализации мембраны Бруха на поверхности опухоли. При исследовании ретинальных изменений необходимо обращать внимание на наличие мелких локальных отслоек РПЭ (первоначально по скатам, при h > 1,2 мм), отслоек нейроэпителия по скатам (при h от 1 мм) с последующим распространением на вершину (при h > 1,5 мм), гиперрефлективных депозитов на уровне РПЭ (h > 1,2 мм), на формирование единого блока хориокапилляры/БМ/РПЭ/фоторецепторы (h > 1,2 мм), по мере роста опухоли необходимо обращать внимание на увеличение количества и укрупнение кист, а также их распространение с вершины на скаты.
ОКТ играет важную роль при планировании органосохранного лечения, при этом неблагоприятными прогностическими признаками являются крупные интраретинальные полости, крупные интраретинальные кисты, интраретинальный отек, скопление транссудата над опухолью, наличие отслойки нейроэпителия над опухолью и за ее пределами, разрыв слоя фоторецепторов.
С заключительным докладом на тему «Современные направления профилактики прогрессирования миопии» выступил д.м.н. А.В. Мягков.
Материал подготовил Сергей Тумар