К.м.н. В.Д. Ярцев
К.м.н. В.Д. Ярцев представил доклад «Диагностика дакриоцистита». Диагностика дакриоцистита на сегодняшний день не включена в протоколы клинических рекомендаций ни в России, ни в других странах, что по мнению автора может быть связано с многогранностью заболевания.
Дакриоцистит не имеет патогномоничных жалоб: выраженное слезотечение, слизисто-гнойное отделяемое, гиперемия, образование во внутреннем углу глазной щели. Заболевание может протекать и без этих жалоб. Для подтверждения диагноза «дакриоцистит», необходимо доказать отсутствие проходимости слезоотводящих путей, при этом следует иметь в виду, что существуют дакриоциститы с частичной проходимостью слезоотводящих путей. Во всех случаях следует проводить эндоскопическое исследование полости носа, что позволит определить хирургическую тактику.
Золотом стандартом диагностики дакриоциститов является рентгенодиагностика, при этом рекомендуется применение жирорастворимого рентгеноконтрастного препарата, при цифровой дакриорентгенографии ‒ водорастворимого рентгеноконтрастного препарата. Способами введения рентгеноконтрастного препарата являются канюлирование, инстилляции. В НИИГБ им М.М. Краснова всем пациентам проводится компьютерная томография слезоотводящих путей. Перед проведением хирургического вмешательства необходимо оценивать состояние слезного мешка, гайморовой пазухи, нижней носовой раковины по данным КТ. Особое значение КТ околоносовых пазух с контрастированием слезоотводящих путей приобретает при вторичном дакриоцистите, когда имеется требующая коррекции патология структур носа, а также особенности ринологической анатомии, влияющие на ход операции. При дифференциальном диагнозе с жидкостными образованиями слезного мешка (кистозное или солидное образование) проводится ультразвуковое исследование.
Таким образом, диагноз «дакриоцистит» строится на сборе жалоб, осмотре больного, однако золотым стандартом остается рентгенодиагностика, благодаря которой в некоторых случаях происходит изменение тактики лечения, в качестве дополнительных методов исследования проводится МРТ и УЗИ слезоотводящих путей.
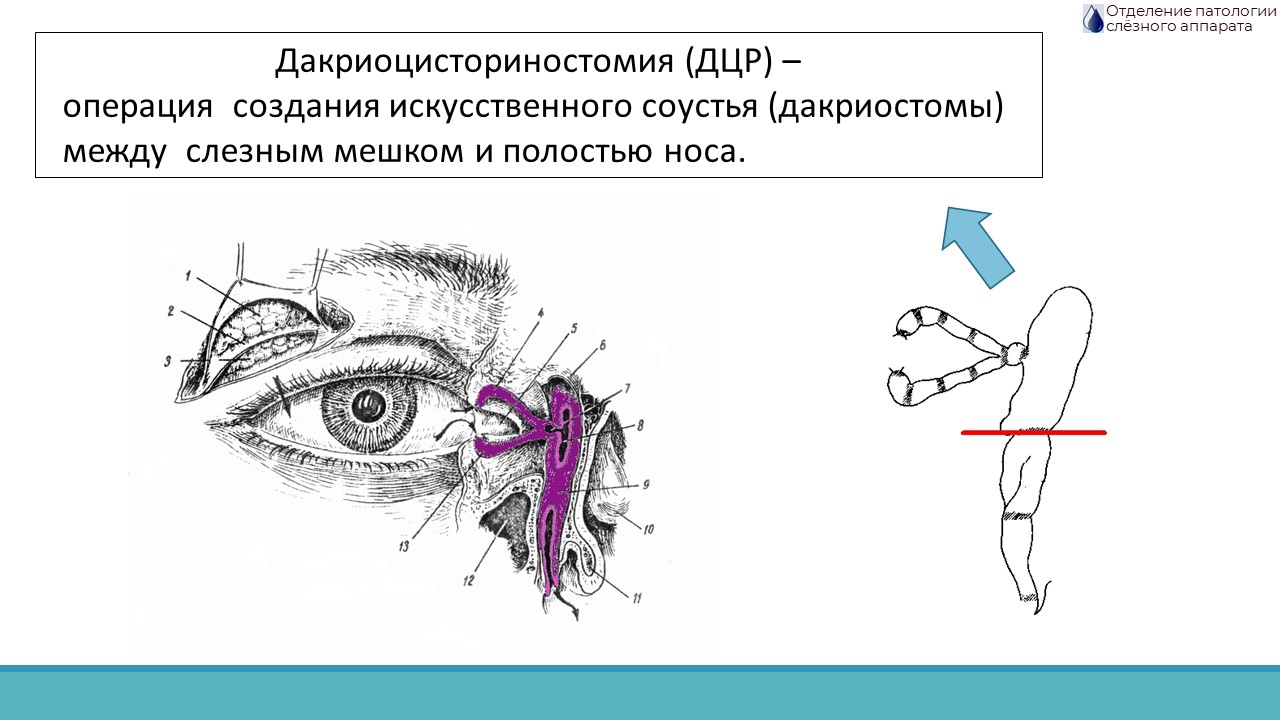
К.м.н. Н.Н. Краховецкий выступил с докладом «Хирургическое лечение дакриоцистита». Самой распространенной операцией при непроходимости вертикального отдела слезоотводящих путей является дакриоцисториностомия (ДЦР) (рис. 1), вмешательство, показанное при нарушении слезного оттока ниже слезного мешка. В недавнем прошлом золотым стандартом в лечении дакриоцистита считалась ДЦР с наружным доступом. Среди «плюсов» метода – широкий доступ к слезному мешку, лучшая визуализация полости слезного мешка, надежное соединение слизистых лоскутов; среди «минусов» – кожный разрез, риск нарушения насосной функции слезных канальцев.
В последние годы методом выбора является эндоскопическая эндоназальная ДЦР (ЭЭДЦР). Преимущества ЭЭДЦР: косметичность, возможность проведения операции в любой стадии флегмонозного дакриоцистита, отсутствие риска нарушения физиологической системы слезоотведения, возможность одномоментного устранения неблагоприятных факторов. К недостаткам методики, по мнению автора, можно отнести высокую стоимость оборудования и наличие специального эндоскопического инструментария.
Этапы ЭЭДЦР: 1. Разрез слизистой оболочки полости носа; 2. Резекция костного фрагмента; 3. Разрез медиальной стенки слезного мешка; 4. Формирование дакриостомы.
Послеоперационный период включает манипуляции: удаление тампонов (губок) из области дакриостомы на 2-е сутки п/о; туалет полости носа под контролем эндоскопа; промывание полости носа солевыми растворами 5-7 раз в сутки в течение 2 месяцев п/о; топические назальные глюкокортикостероиды в течение 1 месяца п/о; промывание слезоотводящих путей растворами антисептиков; инстилляции антибактериальных и далее антисептических глазных капель в течение 1 месяца.
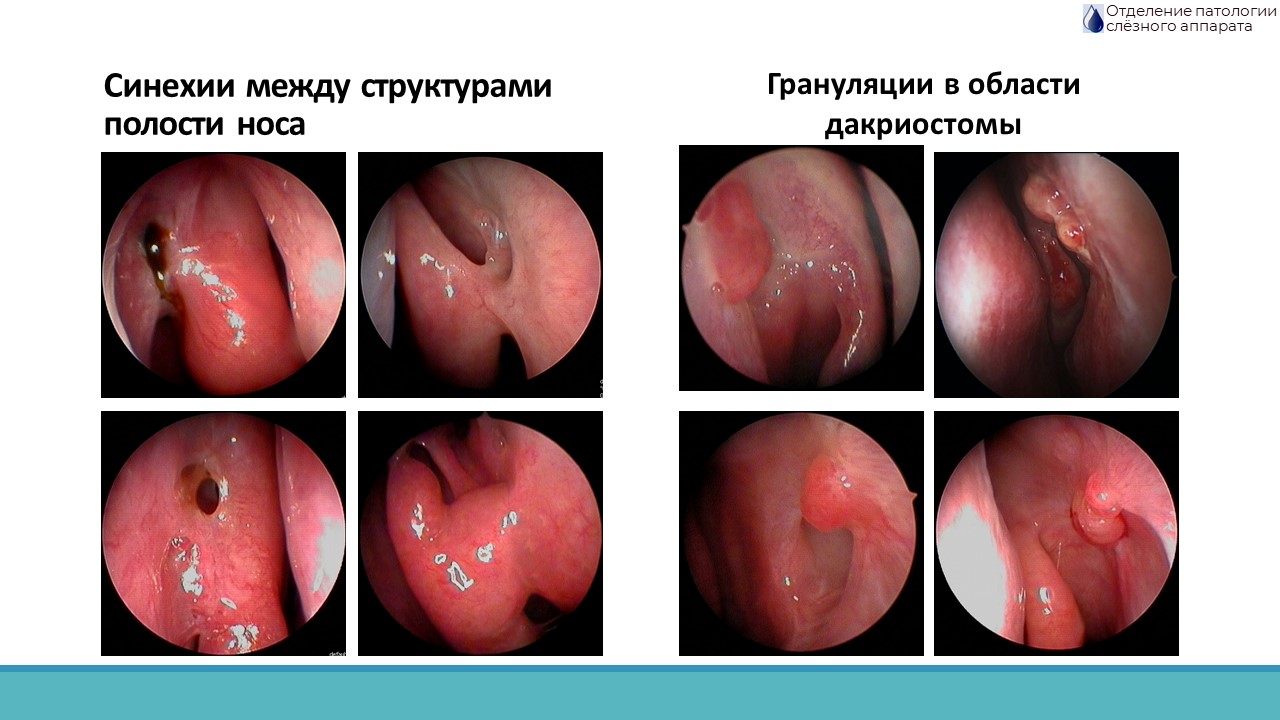
При недостаточном п/о уходе высок риск формирования синехий между средней носовой раковиной и областью дакриостомы, которые могут препятствовать прохождению слезной жидкости, а также грануляций в области дакриостомы (рис. 2), что может явиться причиной рецидива.
По данным на 2016 год, положительные исходы хирургического лечения пациентов с хроническим дакриоциститом с применением методики ЭЭДЦР составили 87,4% из 190 случаев, рецидивы случились в 12,6%.
По данным литературы, причинами рецидива после ЭЭДЦР являются частичное или полное заращение дакриостомы (53,3%), стеноз и облитерация слезных канальцев (24,4%), сочетание факторов (22,3%).
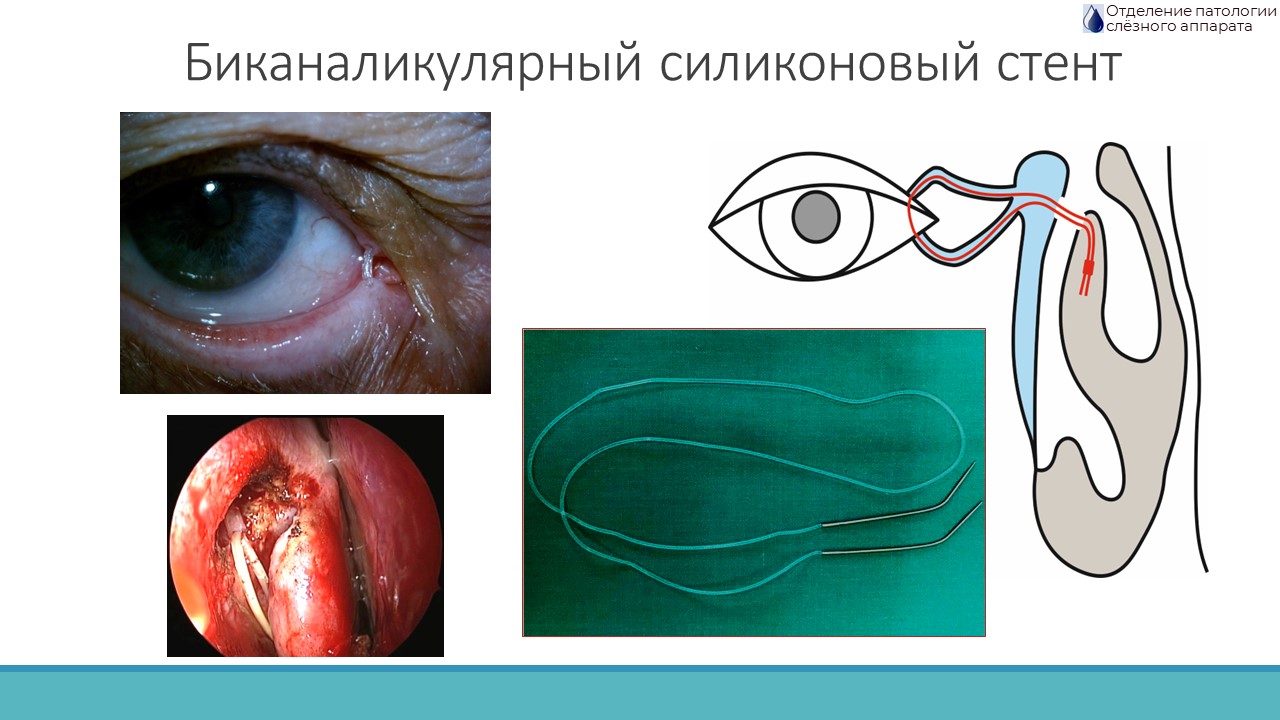
При рубцевании слезных канальцев применяются лакримальные стенты (рис. 3), представляющие собой силиконовую нить или трубку диаметром в 1 мм, к концам которой прикреплены металлические проводники. Использование лакримальных стентов может привести к таким осложнениям, как эпифора на время ношения стента, самопроизвольное смещение стента, эпителиопатия роговицы, токсико-аллергический конъюнктивит, рассечение слезных канальцев, эктопия слезных точек, грануляции в области слезных канальцев, прогрессирование птеригиума. В рутинной практике лакримальные стенты не применяются. Показаниями к их применению являются: дакриоциститы в сочетании со стенозом или облитерацией слезных канальцев или их устья; резкое уменьшение просвета слезного мешка (облитерирующая форма дакриоцистита, рецидив после неэффективной ДЦР).
Подводя итог докладу, к.м.н. Н.Н. Краховецкий обратил внимание на то, что при проведении ЭЭДЦР необходимо обеспечить визуализацию слезных канальцев, резекцию медиальной стенки верхнего отдела носослезного протока, щадящее отношение к слизистой оболочке (сохранение лоскутов); применение силиконовых стентов возможно только по показаниям.

Академик РАН С.Э. Аветисов
С докладом на тему «Нарушения гидродинамики и рефракции как коморбидные состояния» выступил академик РАН С.Э. Аветисов. Коморбидные состояния – одновременное наличие заболеваний, затрудняющее диагностику и усложняющее определение тактики ведения пациента. Основным фактором формирования первичных аметропий высокой степени являются существенные изменения размеров переднезадней оси.
Влияние первичных аметропий на результаты тонометрии. Распространенным принципом измерения ВГД является апланационная тонометрия. Площадь апланации при идентичном уровне ВГД может зависеть от жесткости роговицы. Тенденция к снижению или повышению показателей жесткости усиливается при существенном изменении переднезадней оси. Так при миопии роговица мягче, при гиперметропии – жестче. Таким образом, существует потенциальная зависимость результатов апланационных методов тонометрии от вида клинической рефракции: при гиперметропии происходит завышение данных тонометрии, при миопии – занижение.
Особенности тонометрии после кераторефракционных вмешательств. После радиальной кератотомии (РК) происходит нарушение природной регулярности основных структурно-функциональных показателей роговицы: снижение жесткости роговицы (преимущественно на средней периферии), изменения кривизны и регулярности передней поверхности роговицы – увеличение радиуса кривизны (уплощение) в центральной зоне и уменьшение радиуса кривизны (укручение) – в периферических участках. Результат: недостоверность апланационных методов тонометрии с тенденцией к завышению показателей.
Изменения биомеханических показателей после операции LASIK по поводу миопии: при увеличении объема абляции существенно снижаются роговичный гистерезис и фактор резистентности, что может приводить к занижению показателей тонометрии при применении апланационных методов.
Практические рекомендации: после РК следует применять неапланационный метод (точечная контактная тонометрия на средней периферии роговицы); после лазерной абляции роговицы – использование показателя «роговично-компенсированное ВГД»; в обоих случаях при диагностике и мониторинге глаукомы акцент следует делать на изменения сетчатки и зрительного нерва, а при оценке эффективности гипотензивной терапии – на относительные показатели ВГД, т.е. на степень снижения.
Значение существенных изменений переднезадней оси на формирование и мониторинг нарушений гидродинамики глаза. При существенном уменьшении аксиальной длины (т.н. «короткие глаза») имеют место структурные предпосылки к нарушению гидродинамики (узко- и закрытоугольнвя глаукома): микрокорнеа, мелкая передняя камера, узкий угол передней камеры, относительно большой хрусталик.
Академик РАН С.Э. Аветисов обратил внимание, что на фоне существенного увеличения переднезадней оси может наблюдаться схожесть изменений ДЗН и поля зрения при глаукоме и миопии.
Повышение ВГД в патогенезе индуцированных (вторичных) аметропий. Основными составляющими изменения роговицы после РК являются непосредственно надрезы, силы ВГД, биомеханические параметры роговицы, конкретно, жесткость, т.е. устойчивость к воздействию, изменяющему форму. То есть рефракционный эффект после нанесения надрезов зависит от условного баланса между уровнем ВГД и жесткостью роговицы. У части пациентов, перенесших РК, наблюдается прогрессирующая гиперметропия – сдвиг рефракции в сторону гиперметропии в отдаленные сроки за счет уплощения роговицы в центральной зоне (вследствие повышения ВГД), т.е. фактически происходит усиление рефракционного эффекта операции.
Таким образом, причинами формирования прогрессирующей гиперметропии являются: исходные – индивидуально сниженные биомеханические параметры роговицы; предрасполагающие – неперфорирующие надрезы роговицы, заживление надрезов первого типа; определяющие – возрастные изменения биомеханики роговицы, повышение ВГД. В качестве иллюстрации автор привел пример изменения рефракции роговицы после антиглаукомной операции у пациента, ранее перенесшего РК (рис. 1), что свидетельствует об определяющей роли ВГД в тенденции к сдвигу рефракции в сторону гиперметропии.
Вопросы, требующие решения при клинических проявлениях прогрессирующей гиперметропии после РК: обследование для подтверждения или исключения глаукомы (пациентов с прогрессирующей гиперметропией следует относить к группе риска развития глаукомы); выбор метода оптической коррекции гиперметропии.
Подводя итог, автор отметил, что коморбидность нарушений гидродинамики и рефракции может быть обусловлена изменениями основных компонентов формирования аметропий различного генеза – роговицы и переднезадней оси.
«Осложнения антиглаукомной хирургии глазами поликлинического врача» ‒ тема доклада профессора В.П. Еричева. Факторы, влияющие на частоту и характер осложнений: высокий уровень исходного ВГД, более продвинутые стадии глаукомы, возраст, коморбидные состояния, некорректная предоперационная подготовка, тип хирургического вмешательства, уровень хирургической подготовки врача, корректность послеоперационного ведения, случайные (поведенческие) факторы.
Среди основных осложнений автор привел синдром мелкой передней камеры, цилиохориоидальную отслойку (ЦХО), геморрагические осложнения (гифемы, гемофтальм), асептическое воспаление (ирит, иридоциклит, пластический увеит), наружная фильтрация, офтальмогипертензия, «злокачественная» глаукома, эндофтальмит, набухающая катаракта.