Академик РАН А.Ф. Бровкина (Москва) выступила с докладом на тему «Стероидоустойчивые формы эндокринной офтальмопатии». Термин «эндокринная офтальмопатия» (ЭОП) впервые был предложен R. Graves в 1835 году. Распространенность ЭОП среди европейского населения – 1: 10 000
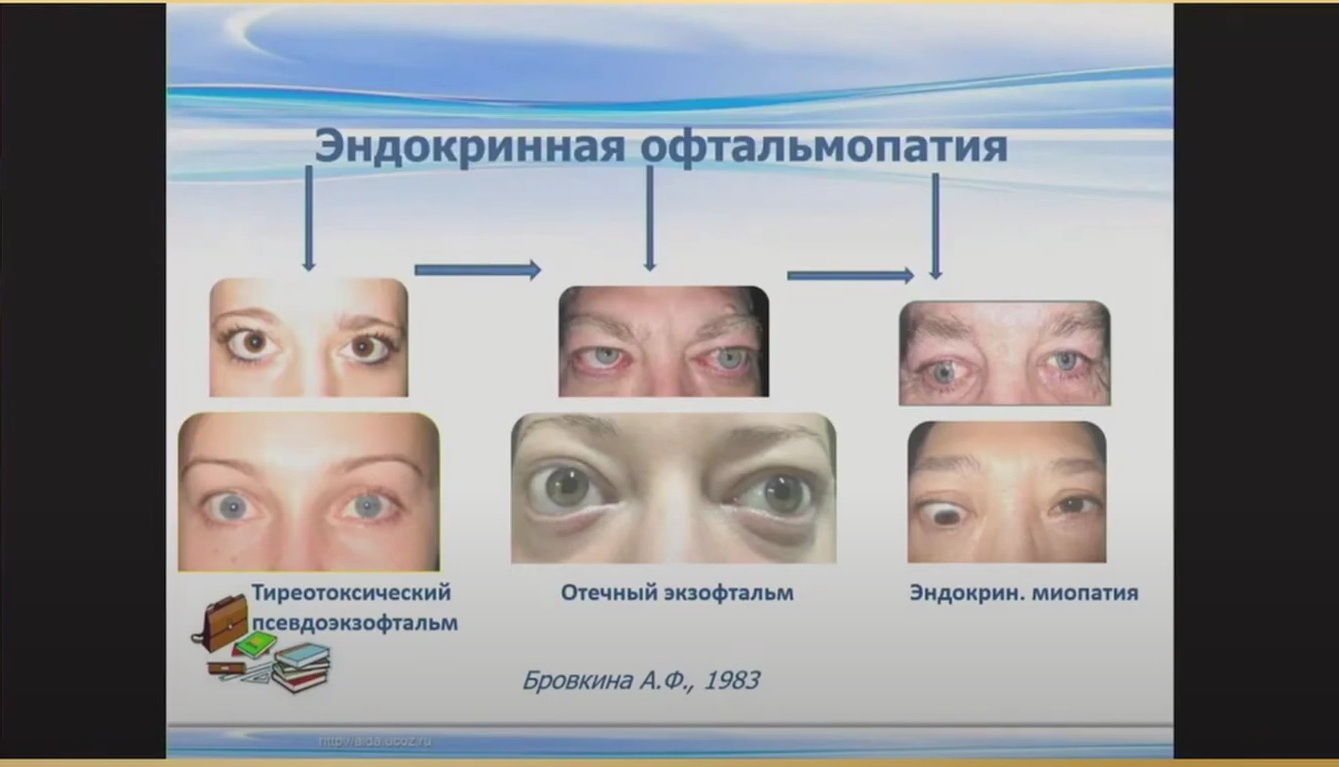
На рис. 1 представлены различные клинические формы ЭОП, переходящие из более легкой формы – в более тяжелую. Наиболее драматичной остается средняя группа ‒ группа больных отечным экзофтальмом (ОЭ), приводящим больных к инвалидизации. В свою очередь ОЭ имеет маргинальные формы: миогенный ОЭ и липогенный ОЭ, а также промежуточную ‒ смешанный ОЭ.
По данными литературы, умеренная и тяжелая форма ЭОП соответствуют миогенному и смешанному ОЭ. По данным литературы, в 2020 году на Тайване около 35% больных ЭОП находились в стадии жесточайшей декомпенсации, т.е. имели миогенный и смешанный ОЭ.
С 1953 года «золотым стандартом» лечения считается применение глюкокортикоидов. Среди вопросов, которые волнуют клиницистов, – неадекватный ответ на лечение. Согласно исследованиям, каждый пятый больной ЭОП не отвечает на предлагаемое лечение, прежде всего это касается липогенного ОЭ. При этом заболевании происходит увеличение объема орбитального жира; течение заболевания имеет монотонный характер при сохранности зрительных функций.
Предположительными причинами формирования ГК-устойчивых форм являются: монотонное, длительное течение, переходящее в фиброз; зрительные функции не страдают; не имеют стадии суб- и декомпенсации.
Среди предположительных причин формирования ГК-устойчивых форм академик РАН А.Ф. Бровкина отметила длительный период заболевания, на заключительном этапе которого элементы аутоиммунного воспаления, возникающие в прямых мышцах глаза и в орбитальной клетчатке, переходят в стадию фиброза, который не поддается лечению ГК. Способ введения. Существует внутривенный способ введения большими дозами, пероральный способ. Проведенные исследования показали, что при применении адекватных, больших доз способ введения не влияет на эффективность лечения. Однако большие дозы ГК могут иметь побочные эффекты (страдает слизистая желудка). Применение низких доз ГК не имеет эффекта. В 2012—2013 году впервые был описан полиморфный маркер гена-рецептора ГК. Было высказано предположение, что отсутствие гена-рецептора формирует группу стероидо-устойчивых форм, однако, отечественные исследователи доказали, что полиморфизм генов к рецептору ГК не имеет значения. Существуют эпигенетические факторы, о которых стало известно в начале XXI века, когда была описана роль микроРНК в развитии различных заболеваний, в т.ч. офтальмологических. Таким образом, доказано, что ЭОП представляет собой аутоиммунное воспаление в мягких тканях орбиты, при этом подчеркнула докладчик, речь идет только о поражении прямых мышц глаза и орбитальной клетчатки, а также накоплении глюкозаминогликанов, при котором орбитальная клетчатка и ткани прямых мышц приобретают способность накапливать жидкость в 5 раз больше по сравнению с нормой. Исследования также показали, что в формировании симптомов ЭОП большую роль играет локальный адипозогенез, в возникновении которого «виноваты» орбитальные фибробласты, которые при появлении направления к патологическим изменениям моментально из спокойного состояния переходят в активную, подвижную, форму и начинают активировать цитокины. На сегодняшний день доказано, что именно орбитальный фибробласт является источником появления новой, дополнительной жировой ткани в орбите.
В настоящее время изучена роль 100 микроРНК. Получены результаты по трем микроРНК, «ответственным» за ЭОП: микроРНК-21, микроРНК-146, микроРНК-155. Две последние участвуют в развитии неспецифического воспалительного процесса в организме человека, в т.ч. в орбитальной ткани.
Роль микроРНК в патогенезе ОЭ и в ответе на ГК терапию. МикроРНК-146: уровень экспрессии снижен – микроРНК принимают участие в пролиферации и дифференцировке клеток через подавление активности Т-лимфоцитов; уровень экспрессии повышен – подавляя клеточный апоптоз, микро РНК-146 увеличивают жизнеспособность и митоз орбитальных фибробластов, их дифференцировку в адипоциты, ингибирует продукцию ГАГ. МикроРНК-155: регулируют развитие регуляторных Т-лимфоцитов и их конкурентоспособность, усиливают воспаление, подавляя передачу сигналов цитокинов, подавляют дифференцировку адипоцитов. На рис. 2 представлен уровень экспрессии микроРНК-146а и микроРНК-155 в плазме крови больных ЭОП. Показано, что обе микроРНК усиливают свою экспрессию в группе больных с липогенным вариантом. Автор обратила внимание, что у больных миогенной и смешанной формой ОЭ экспрессия микроРНК увеличивается в среднем в 7-8 раз, у пациентов с эндокринной миопатией (ЭМ), уже имеющих элементы фиброза, уровень экспрессии микроРНК выше, у больных липогенным вариантом происходит выброс микроРНК.
Стали понятны эпигенетические механизмы, участие микроРНК, которые активизируя экспрессию, действуют на орбитальные фибробласты, стимулируют формирование адипозогенеза и устойчивость к ГК.
В заключение академик РАН А.Ф. Бровкина подчеркнула, что нельзя начинать лечение с низких доз ГК препаратов, это не дает результата и наносит вред больным.
Таким образом, обоснованы причины формирования стероидоустойчивых форм ЭОП; эпигенетически подтвержден липогенный вариант отечного экзофтальма, обосновано его патогенетически ориентированное хирургическое лечение (внутренняя декомпрессия орбиты).
В заседании также выступили профессор Е.А. Егоров (Москва), его доклад касался современных подходов в лечении глаукомной оптической нейропатии, и профессор В.В. Страхов (Ярославль) с докладом на тему «Ретинальный вектор в патогенезе первичной глаукомы».
Материал подготовил Сергей Тумар