И.Э. Иошин, А.И. Толчинская, И.В. Максимов, А.В. Ракова
ФГБУ «Клиническая больница» Управления делами Президента Российской Федерации
Важное место в современной офтальмологии занимает вопрос лечения глаукомы. Глаукома – это социально-значимое заболевание, которое может приводить к необратимой слепоте [1-5]. Одним из ведущих направлений в ее лечении является снижение внутриглазного давления (ВГД), которое достигается путем назначения гипотензивных препаратов, использованием лазерных технологий, а также применением антиглаукомных операций проникающего и непроникающего типов. [1-4]. Однако при развитой и далекозашедшей стадии глаукомы при хирургическом лечении заболевания гипотензивный эффект не всегда стабилен. Выраженная фибропластическая активность тканей глаза приводит к процессам рубцевания и облитерации сформированных в ходе операции путей оттока водянистой влаги [3]. В связи с этим развивается тяжелая форма глаукомы – рефрактерная (РГ), сопровождающаяся устойчивостью к проводимым традиционным методам лечения [1-4].
В качестве альтернативы традиционным методам лечения рефрактерной глаукомы была предложена непрерывная диод-лазерная циклофотокоагуляция (ЦФК) с длиной волны 810 нм, направленная на подавление продукции водянистой влаги. Но использование высокоинтенсивного лазерного воздействия сопровождалось коагуляционным некрозом цилиарного тела, что, с одной стороны, обладало достаточным гипотензивным эффектом, но с другой ‒ ограничивало применение данной методики из-за часто возникающих осложнений после процедуры, что определило его как метод лечения терминальной глаукомы. [3-5].
Появление микроимпульсного режима открыло новые горизонты в лазерной офтальмохирургии. Клиническое использование технологии микроимпульсных диодов было впервые исследовано в конце 1990-х годов. Технология показала свою эффективность при лечении заболеваний сетчатки, включая кистозный макулярный отек, диабетической ретинопатии (Moorman & Hamilton, 1999), центральной серозной хориоретинопатии (Lanzetta et al. 2008). В 2010 году Tan и соавт. опубликовали в Сингапуре первое исследование по применению этой технологии при лечении рефрактерной глаукомы. Доказанная эффективность и отсутствие осложнений в раннем и длительном послеоперационном периоде вызвали интерес к данной методике [16].
Принципиальное отличие микроимпульсной циклофотокоагуляции от непрерывной заключается в использовании циклического лазерного излучения. Микроимпульсный диодный лазер с длиной волны 810 нм чередуется между периодами лечения (импульсы ‒ циклы включения) и периодами покоя (время термической релаксации ‒ циклы выключения). Циклы выключения предотвращают повышение температуры, поэтому не возникает теплового эффекта, как в непрерывном режиме, что исключает возникновение коагуляционного некроза. Благодаря применению циклического излучения период включения позволяет накапливать энергию в пигментированном ресничном эпителии, а паузы позволяют соседним непигментированным эпителиальным клеткам остывать и сохранять температуру ниже порога фотокоагуляции [11, 12].
Научными работами и клиническим опытом как в пилотных, так и в рандомизированных исследованиях по лечению РГ было показано, что микроимпульсная циклофотокоагуляция эффективно снижает ВГД с минимальными осложнениями [6-10, 13-17]. Данные работы определили возможности использования микроимпульсной циклофотокоагуляции в качестве эффективной и безопасной процедуры в лечении различных стадий глаукомы [13-15].
Для оценки совокупного вероятного успеха лазерного лечения после операции используется статистический метод Каплана-Мейера [13, 15]. Основными параметрами успеха авторы определяют следующие: показатели внутриглазного давления между 6 и 21 мм рт. ст. на фоне гипотензивных препаратов или без них; снижение ВГД на 20% и более от базового внутриглазного давления после 3 послеоперационных месяцев; отсутствие осложнений и отсутствие необходимости в дополнительной хирургии глаукомы, за исключением мЦФК.
В литературе подчеркивается, что с учетом стадии заболевания повторная операция мЦФК может считаться запланированным следующим этапом лечения, а кратность процедуры может быть различной [16]. Обсуждаются вопросы длительности гипотензивного эффекта после первоначально проведенной мЦФК в зависимости от стадии и типа глаукомы, возможность и сроки проведения повторной мЦФК, а также выбор мощности лазерной энергии, особенно при повторном вмешательстве [14-17].
Цель: оценить результаты повторной микроимпульсной циклофокоагуляции (мЦФК) у пациентов с рефрактерной глаукомой (РГ).
Материал и методы. Под наблюдением находилось 80 пациентов (48 мужчин и 32 женщины) в возрасте 74,1±5,9 лет с развитой (15), далекозашедшей (51) и терминальной (14) стадией рефрактерной глаукомы. Длительность заболевания составляла от 3 до 25 лет (в среднем 12,5±4,6 лет), у большинства (52) составляла более 10 лет. Все пациенты перенесли неоднократно антиглаукоматозные лазерные (в среднем 1,3±0,6) и хирургические (в среднем 1,75±0,7) операции проникающего и непроникающего типа и находились на максимальном местном гипотензивном режиме (в среднем 3,1±0,4 препарата).
До и после операции мЦФК всем пациентам проводилось офтальмологическое обследование, включающее визометрию, тонометрию (пневмо- и по методу Маклакова), биомикроскопию, компьютерную периметрию и оптическую когерентную томографию. Полученные данные обобщены в таблице 1.
Табл. 1. Общие предоперационные показатели у пациентов с глаукомой (n=80)
| Стадия глаукомы | Возраст | Количество
операций в анамнезе |
МКОЗ | ВГД | Количество гипотензивных
препаратов |
| II стадия (n=15) | 68,0±8,6 | 1,7±0,6 | 0,71±0,11 | 28,3±8,5 | 2,7±0,3 |
| III стадия (n=51 | 75,0±7,2 | 2,1±0,4 | 0,45±0,12 | 30,1±7,2 | 3,0±0,4 |
| IV стадия (n=14) | 78,0±6,3 | 2,3±0,5 | 0,003±0,001 | 33,9±8,3 | 3,2±0,5 |
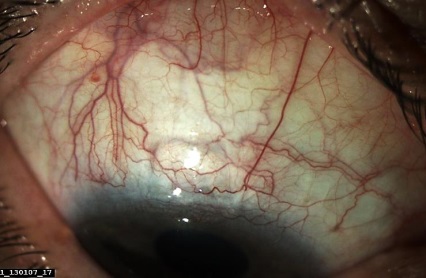
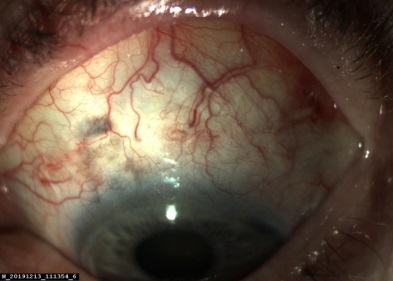
До операции у пациентов глаза были спокойны. У части больных отмечалась застойная инъекция глазного яблока, рубцовые изменения конъюнктивы в зоне ранее выполненных хирургических антиглаукомных вмешательств, фильтрационная подушка была облитерирована (рис. 1).
Рис. 1. Глаза пациентов с развитой (а), далекозашедшей (б) и терминальной (в) стадией рефрактерной глаукомы после перенесенных антиглаукомных операций.
Оптическую когерентную томографию (ОКТ) заднего отрезка глазного яблока выполняли на приборе OCT-2000 3D (Topcon). При обследовании оценивали состояние диска зрительного нерва и макулярной зоны сетчатки: толщину слоя нервных волокон в перипапиллярной зоне, толщину сетчатки в макулярной области. Компьютерную периметрию (Octopus 900) проводили больным со второй и третьей стадией заболевания.
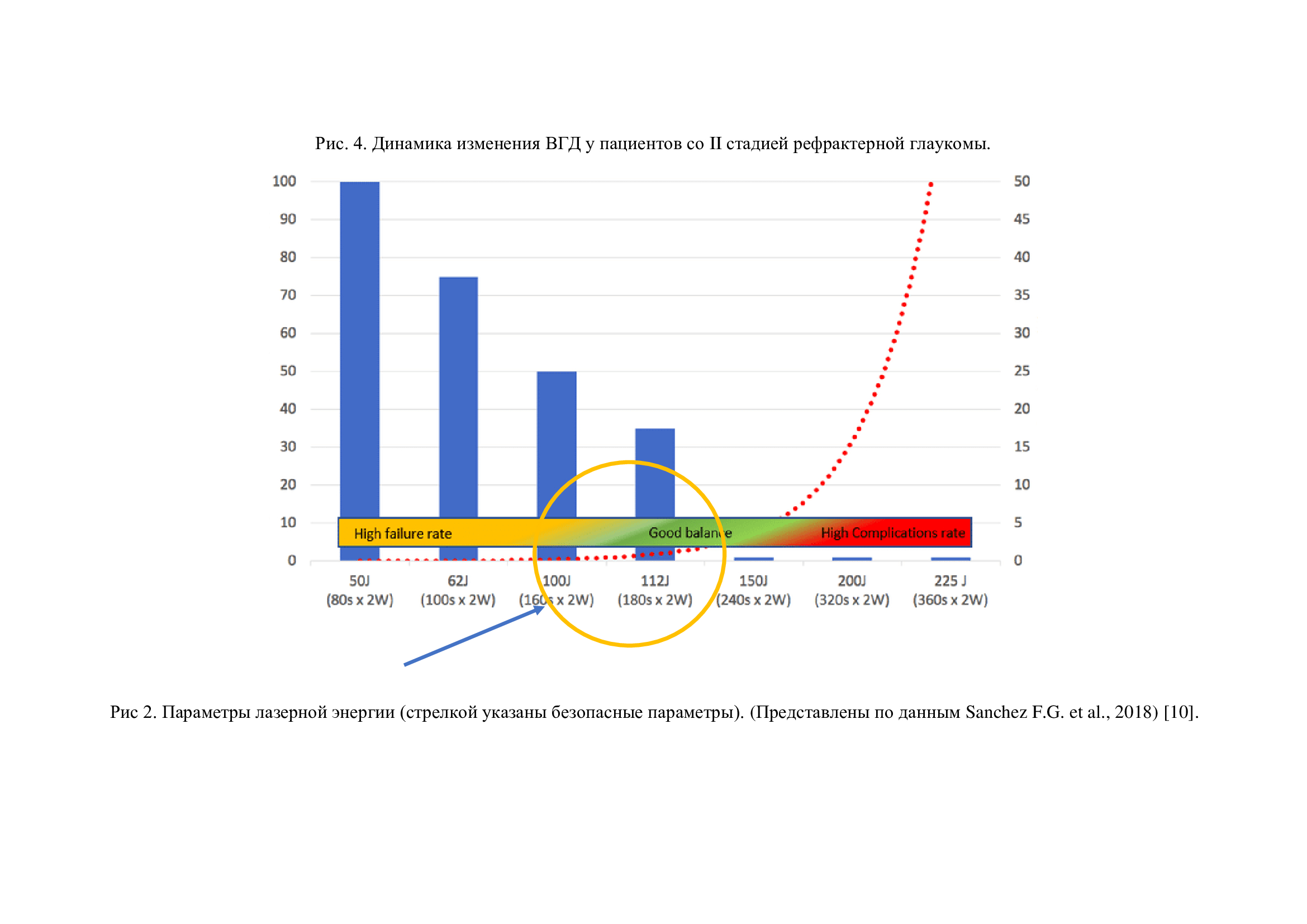
Техника операции: Процедура мЦФК выполнялась с использованием прибора SUPRA 810 (Quantel Medical, Франция). Независимо от стадии глаукомы во время первой процедуры применялись базовые параметры лазера: мощность ‒ W=2 Вт, скважность – 31,3%, время воздействия на обе полусферы — 160 сек. Общая энергия лазерного воздействия, рассчитанная по формуле (E= 2W х рабочий цикл 31,3% х время воздействия ©), составила 100 Дж. Проведение повторной (после первой операции) процедуры планировалось в случаях, если значения ВГД выше 21 мм рт.ст. или процент снижения ВГД от исходного меньше 20% к сроку последнего контрольного осмотра. Во время повторной процедуры мЦФК лазерная энергия были увеличена до 125 Дж путем увеличения времени лазерного воздействия ‒ 200 сек. Указанные режимы с энергией лазерного воздействия находятся в безопасной и эффективной зоне в пределах от 100 до 150 Дж при проведении мЦФК (рис. 2) [13].
Рис 2. Параметры лазерной энергии (стрелкой указаны безопасные параметры). (Представлены по данным Sanchez F.G. et al., 2018) [12]