Однако до сих пор не установлены четкие общепринятые критерии проведения ЛК разрывов, что заставляет лазерных хирургов решать этот вопрос, полагаясь главным образом на собственный опыт. Мы со своей стороны считаем, что благоприятное течение обусловлено топографическими соотношениями базиса стекловидного тела и периферической сетчатки, когда неповрежденный корковый слой тампонирует разрывы сетчатки [2].
В некоторых работах встречаются указания на различие естественной эволюции ретинальных разрывов в зависимости от их типа. Так, в частности, из работы [16] следует, что наиболее часто встречающиеся округлые (атрофические) отверстия сетчатки редко прогрессируют при наличии сопутствующих факторов риска: «решетчатой» дегенерации, «парных» глаз, наличии субклинической ОС. В то же время клапанные разрывы достаточно часто приводят к ОС, поскольку находятся под действием тракционных сил, в особенности при возникновении неполной задней гиалоидной отслойки (ЗГО). При оценке возможности прогрессирования ретинальных разрывов придается большое значение такому фактору риска, как высокая миопия. Поскольку прогрессирование миопии приводит к нарастанию дистрофических изменений периферии сетчатки, этот фактор при выборе тактики лечения ретинальных разрывов относится к прогностически неблагоприятным [14]. С другой стороны, высказывается мнение [20, 29], что завершенная отслойка заднегиалоидной мембраны, которая часто сопутствует высоким степеням близорукости, является благоприятным прогностическим признаком, поскольку разрывы на ее фоне освобождены от тракционного действия коркового слоя стекловидного тела.
В выборе показаний к ЛК сетчатки при ретинальных разрывах играет роль наличие или отсутствие клинических симптомов. Ряд авторов [7, 18] рекомендуют проводить ЛК при всех формах симптоматических разрывов сетчатки.
Обращает на себя внимание мнение некоторых исследователей о нецелесообразности проведения ЛК вокруг больших клапанных разрывов, локализующихся в верхних отделах глазного дна [9, 26], для этой цели предлагают использовать криопексию или пломбирование. Однако, по мнению других авторов [15, 21], лазерные ограничивающие вмешательства эффективны при клапанных разрывах вне зависимости от их локализации. Мы полагаем, что эволюция разрыва зависит не от верхнего или нижнего его расположения, а от локализации последнего относительно основания стекловидного тела и топоанатомических соотношений коркового слоя стекловидного тела и сетчатки.
Для блокирования круглых разрывов некоторые авторы [19] не рекомендуют применять ЛК, отдавая предпочтение другим методам (криопексия, склеральное пломбирование). Наши наблюдения показали, что в отношении разрывов сетчатки, не превышающих в размерах одного квадранта (при отсутствии клинической отслойки сетчатки), эффективность метода имеет тенденцию к снижению [5] с нарастанием размера отграничиваемого дефекта.
Шварты стекловидного тела нередко обуславливают локальное тракционное действие на край разрыва и служат в этих случаях причиной отслойки сетчатки. Тяжи стекловидного тела, прикрепляющиеся у вершины клапана, определяемые офтальмоскопически, формируют его характерный вид (с завернутыми краями) при отсутствии завершенной ЗГО, могут снижать терапевтическую эффективность лазерных отграничивающих вмешательств. Из приведенного выше анализа факторов риска вытекает, что на терапевтическую эффективность отграничивающей лазерной коагуляции при разрывах сетчатки оказывает влияние лишь один фактор — тракционное действие шварт стекловидного тела по краю разрыва при отсутствии завершенной ЗГО.
В последние годы расширились показания к профилактической ЛК в связи с эксимерной коррекцией аномалий рефракции (LAZIK). При проведении кератомилеза ВГД кратковременно повышается до 60 мм рт.ст., что требует надежного закрытия не только разрывов сетчатки, но и периферических дегенераций.
Анализ современной литературы и наши собственные наблюдения [2, 8] позволяют выделить группу абсолютных показаний к проведению отграничивающей ЛК при разрывах сетчатки:
1) все типы разрывов при наличии выраженной тракции их края;
2) симптоматические клапанные разрывы;
3) разрывы в афакичных глазах;
4) все типы разрывов с наличием субретинальной жидкости, распространяющейся свыше 1 диаметра ДЗН (ДД) от края разрывов;
5) все типы разрывов протяженностью более 30° (или 1 часа по меридиану);
6) все типы разрывов на парных глазах при односторонней отслойке сетчатки;
7) разрывы и периферические дегенерации с недоброкачественным течением перед операцией LAZIK.
«Вторые» глаза при односторонней отслойке сетчатки относятся к глазам повышенного риска, так как частота возникновения отслойки в них доходит до 44,9% [22, 31]. Это обусловлено целым рядом факторов: наследственными гиалоидоретинопатиями, наличием близорукости и дегенераций, а нередко и разрывов сетчатки, непрямой травмой и т.п.
Наиболее эффективным методом активной профилактики ОС является лазеркоагуляция, показания к которой в связи с этим значительно расширяются. Мы считаем целесообразным проводить ЛК не только симптоматических, но и асимптоматических разрывов, хориоретинальных дистрофий с недоброкачественным течением, а также других дистрофий с наличием в них тракционного компонента, прогрессирующего ретиношизиса без или при прорыве линии самоограничений. В этих случаях при проведении лазеркоагуляции сетчатки рекомендуется использовать минимально низкие уровни энергии, необходимой для получения коагулятов с одновременным увеличением площади коагуляции (в 2-3 раза), что позволяет снизить частоту отслоек до минимума [8].
Можно предположить, что при более жесткой коагуляции происходит повреждение корковых отделов стекловидного тела с возникновением его сокращения и более выраженной тракции сетчатки вследствие сращения гиалоидной мембраны с последней.
Повышение уровня диагностического обследования больных при правильно определенных показаниях к профилактической коагуляции позволяет свести до минимума частоту возникновения отслоек на «парных» глазах.
Лазерное лечение отслоек сетчатки
При уже свершившейся отслойке сетчатки нередко проводится комбинированное хирургическое и лазерное лечение. Основной целью хирургии отслоек сетчатки является достижение ее анатомического прилегания для сохранения или улучшения зрительных функций оперированного глаза. Роль экстрасклерального пломбирования (ЭСП) наряду с эндовитреальными методами лечения трудно переоценить (прилегание сетчатки достигается в 95-98%). Функциональные результаты до сих пор оставляют желать лучшего. Даже после успешно проведенных операций по поводу ОС, не распространяющихся на макулярную область, нередко отмечается заметное снижение остроты зрения оперированного глаза [9]. Основными причинами в этих случаях бывают отек сетчатки в макулярной области, ухудшение кровоснабжения сетчатки, микроскладчатость, затекание и медленное рассасывание субретинальной жидкости (СРЖ), дистрофия сетчатки в макулярной области вследствие смещения последней в сторону пломбы и др. Таким образом, стремление к наиболее надежному и гарантированному анатомическому успеху (увеличение объема экстрасклерального пломбирования, постоянного вдавления, субтотальное дренирование СРЖ, массивная криоретинопексия) часто приводит к существенному ухудшению визуальных исходов и повышению вероятности рецидивов в результате развития обширной витреоретинальной ретракции. При тенденции, направленной на сокращение объема операции (временное вдавление надувными баллонами, бездренажные операции, бескоагуляционные операции локального экстрасклерального пломбирования), снижается надежность операции.
При уменьшении травматичности операции с целью улучшения визуальных результатов возрастает риск возникновения рецидивов из-за разблокирования РР.
Совершенствование хирургических методов лечения в комбинации с современным научно обоснованным подходом к использованию ЛК у хирургических больных в до- и послеоперационном периодах позволяет существенным образом уменьшить как риск таких осложнений, как рецидивы ОС, так и снижение функциональных результатов [4, 30].
Нами была разработана схема поэтапной ЛК, проводимой в до- или послеоперационном периодах у хирургических больных, максимально учитывающая основные факторы риска возникновения рецидивов ОС, а также возможность сохранения и даже повышения остроты зрения у больных с ОС [3].
Тактика выполнения ЛК зависела от отсутствия или распространения ОС на центральные отделы.
I этап — в предоперационном периоде проведение лазерного барража макулярной зоны у больных с ОС, не захватывающей макулярную область, с целью профилактики затекания СРЖ, что позволяет снизить риск макулярного фиброза и сохранить высокую остроту зрения.
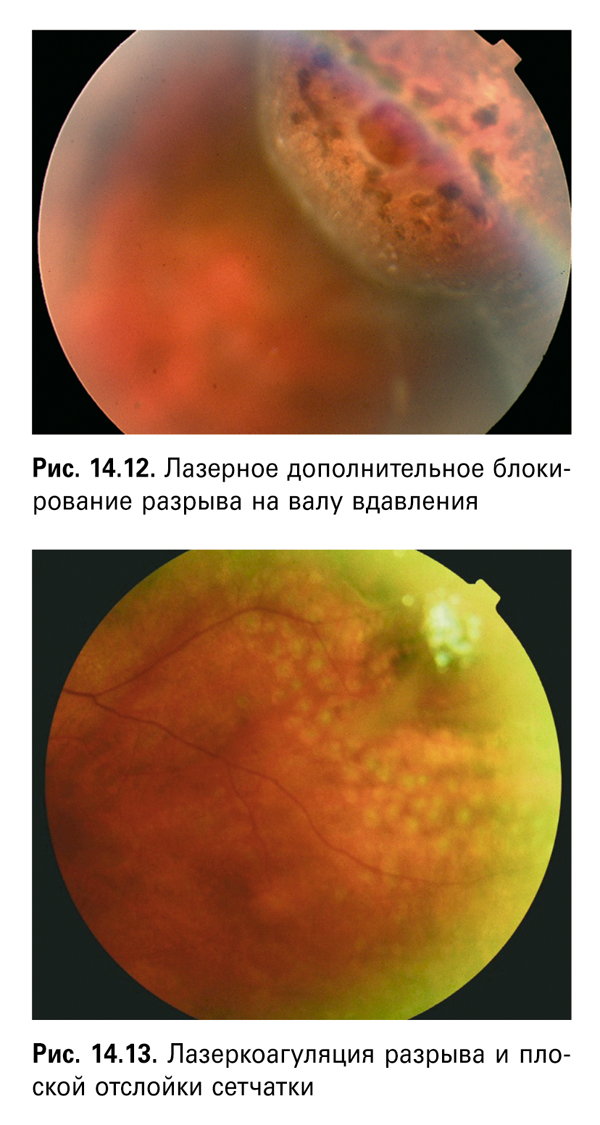
II этап — в послеоперационном периоде ЛК вокруг разрыва на валу вдавливания повышает надежность блокирования РР пломбой меньшего размера (рис. 14.12).
III этап — ЛК центральнее вала вдавливания или парамакулярный барраж с целью повышения остроты зрения в послеоперационном периоде (профилактика послеоперационного затекания СРЖ, дистрофии макулярной области вследствие смещения сетчатки в сторону пломбы и формирования микроскладчатости, макулярного отека).
IV этап — лазеркоагуляция «опасных» зон в других отделах сетчатки оперированного глаза позволяет отказаться от циркляжа во время операции (циркляж существенно снижает функциональные результаты).
V этап — лазерная ретинотомия основания клапанного ретинального разрыва с целью ослабления витреоретинальной тракции и уменьшения риска ретракционного рецидива отслойки сетчатки.
Выполнение ЛК преследовало следующие цели:
1) сохранение высокой остроты зрения путем «барража» макулы;
2) закрепление эффекта операции и создание прочной хориоретинальной спайки в зоне разрыва на валу и под валом вдавливания;
3) повышение остроты зрения в послеоперационном периоде путем предупреждения или уменьшения макулярного отека, микроскладчатости;
4) предупреждение рецидива ОС на оперированном глазу с помощью коагуляции «опасных» зон;
5) ослабление витреоретинальной тракции методом лазерной ретинотомии основания клапана.
 Итак, есть основания считать, что в настоящее время сложились все условия для разработки оптимальной тактики лечения больных первичной отслойкой сетчатки, к определению показаний к тому или иному методу хирургического и поэтапного лазерного лечения с максимальным учетом факторов риска рецидивов отслойки сетчатки.
Итак, есть основания считать, что в настоящее время сложились все условия для разработки оптимальной тактики лечения больных первичной отслойкой сетчатки, к определению показаний к тому или иному методу хирургического и поэтапного лазерного лечения с максимальным учетом факторов риска рецидивов отслойки сетчатки.
Лазерная коагуляция сетчатки как самостоятельный метод лечения ОС до настоящего времени имеет очень ограниченное применение и используется в основном для лечения небольших плоских ОС, локализирующихся в пределах одного квадранта, и отслоек с разрывами, прилегающих после постельного режима. В последние годы сотрудниками нашего института проводились работы, направленные на расширение показаний к лазерной коагуляции как самостоятельному методу лечения ОС [5, 6].
Проведенные исследования позволили выявить, что ЛК как самостоятельный метод является достаточно эффективной для лечения следующих видов ОС:
• субклинической локальной ОС протяженностью до 1 ДД от края разрыва (стадия А);
• свежей подвижной отслойки, занимающей не более одного квадранта (стадии А, В);
• малоподвижной локальной ОС (стадия В) с тенденцией к прилеганию на фоне постельного режима;
• частичной самоотграничивающейся отслойки (стадии В, С1).
Преимуществом данного метода является неинвазивность и более высокие функциональные результаты, что делает его приоритетным в лечении вышеуказанных видов ОС (рис. 14.13).






