Имеются два варианта рабочих частей лазера, при помощи которых осуществляется докинг. Это однокомпонентные (LenSx, LensAR), когда головка лазера со сменным интерфейсом непосредственно контактирует с глазом больного и фиксируется к нему при помощи вакуума. И двухкомпонентные (Victus, Catalys) — предполагающие предварительное наложение вакуумного кольца, к которому пристыковывается лазерная головка. В первом варианте стыковка с глазом происходит быстрее, во втором — требуются дополнительные манипуляции, однако при этом, с нашей точки зрения, облегчается докинг в условиях, когда анатомические параметры глаза или лицевого скелета пациента имеют существенную девиацию от среднестатистических.
Характерным последствием лазерного этапа операции является миоз. Последний зависит от ряда факторов: сопутствующая офтальмопатология, медикаментозный режим, время ожидания второго (хирургического) этапа, величина лазерной энергии, работа лазера в непосредственной близости от края зрачка и ряд других. В нашей серии данную проблему в той или иной степени встречали примерно у трети пациентов. Очевидно, сужение зрачка на этапе экстракции катаракты предоставляло хирургу определенные технические трудности.
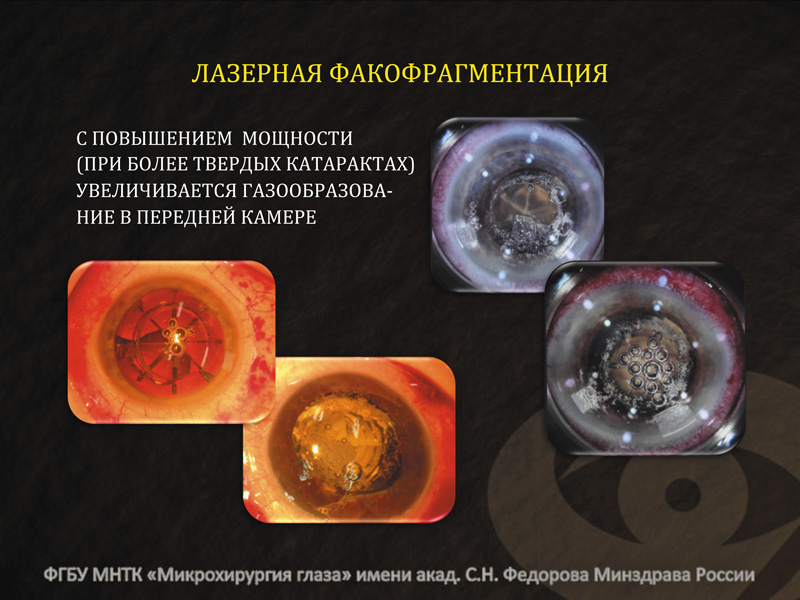
Выполнение лазерного капсулорексиса и фрагментации ядра сопровождаются интенсивным газообразованием рис. 5. Объем пузырьков газа взаимосвязан с энергетическими параметрами. Возможное воздействие данных пузырьков на эндотелий пока не очевидно, однако в начале операции требуется их эвакуация из передней камеры, что осуществляют, как правило, при помощи вытеснения вискоэластиком.
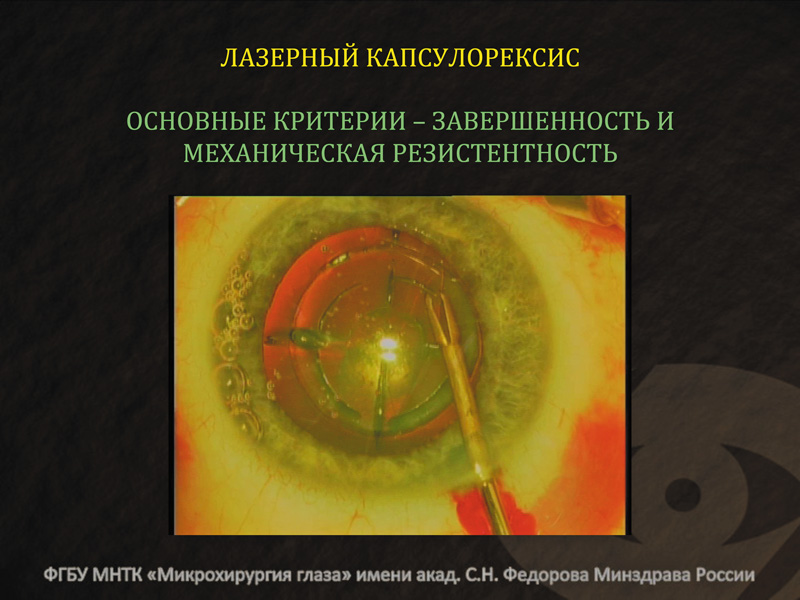
Что касается лазерного капсулорексиса, то это один из критически важных этапов операции. По нашему опыту, использование системы Victus обеспечивало практически в 100% случаев свободное отделение лоскута капсулы от ее периферических отделов. Так, даже у пациента после радиальной кератотомии, где мы ожидали найти выраженные перемычки капсулорексиса из-за экранирующего действия рубцов, таковых практически не было рис. 6.
При использовании системы LenSx, качество просечения передней капсулы было худшим, что характеризовалось необходимостью мануального завершения капсулорексиса при помощи пинцета, служащего для разрыва перемычек. По информации производителя (Alcon), новый интерфейс, снабженный мягкой контактной линзой, позволяет существенно повысить производительность лазерного капсулорексиса и лишен вышеуказанного недостатка.
При гистологическом исследовании капсул, забранных в ходе операции, на большом увеличении (х400) светового микроскопа видно, что край лазерного капсулорексиса напоминает край «почтовой марки». Это отличает его от механического капсулорексиса, край которого имеет ровную поверхность даже при электронной сканирующей микроскопии. Форма края, с нашей точки зрения, не может не сказываться на механической прочности лазерного капсулорексиса. Нам встретилась всего одна работа, посвященная механической прочности капсулорексиса, в которой автор утверждает, что фемтолазерная технология ее не снижает. На наш взгляд, такое утверждение не вполне очевидно и требует дальнейшей верификации.
К преимуществам капсулорексиса выполненного фемтолазером, которые подчеркивают сторонники технологии, относятся ровная и идеально циркулярная форма края капсулы, а также возможность выполнения его с высокой повторяемостью. Действительно, стандартная девиация размера капсулорексиса от планируемого составляет всего 30 микрон, тогда как при мануальном капсулорексисе — на порядок выше. Лазерный капсулорексис дает возможность более точно и предсказуемо достичь прикрытия периферии оптики интраокулярной линзы листком передней капсулы. Последнее представляет собой непременный атрибут современной техники факоэмульсификации, способствующим профилактике вторичной катаракты и более равномерному фиброзированию капсульного мешка.
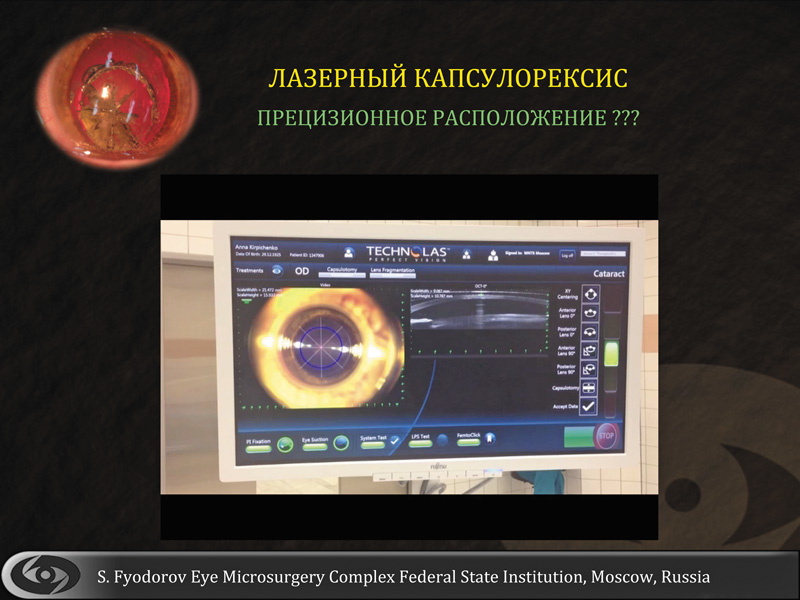
Остается, тем не менее, открытым вопрос: «А обеспечивает ли прецизионное соблюдение размеров и лучшая центрация капсулорексиса более высокий функциональный результат?» Гипотетически, более точная рефракция достигается за счет лучшего прогнозирования положения интра-окулярной линзы в глазу вдоль оптической оси глаза (ELP — эффективное положение линзы), меньшей ее децентрации и наклона. Оптимальная центрация линзы ведет к максимальной реализации ее полезных оптических свойств, что, конечно, в наибольшей степени касается асферических и мультифокальных конструкций.
В этой связи уместно привести результаты исследования, которое было проведено О. Финдлом в начале этого года. Он сравнил механический капсулорексис, выполненный 9 хирургами на 635 глазах, и оценил влияние параметров капсулорексиса на финальные зрительные функции. Пациентов наблюдали на протяжении 2-х месяцев после операции. Выводы автора заключались в отсутствии взаимосвязи нарушений формы и размеров переднего кругового капсулорексиса и положения ИОЛ, глубины передней камеры, децентрации ИОЛ, а также конечного рефракционного результата операции. Японские исследователи также придерживаются мнения, что не существует корреляции между биометрическими параметрами капсулорексиса и рефракционными результатами.
Таким образом, на сегодняшний день можно утверждать, что прецизионное расположение и идеальная форма капсулорексиса, к сожалению, пока не выливаются в ощутимые функциональные преимущества для пациентов. Соответственно преимущества лазерного капсулорексиса на сегодняшний день не очевидны, и возможно их еще только предстоит доказать.
Несколько слов о центрации капсулорексиса. На рис. 7 видно, что центрировать капсулорексис можно по зрительной оси, по центру передней капсулы, по лимбу или по зрачку. Какой из перечисленных вариантов наиболее рационален — еще только предстоит определить. Таким образом, можно констатировать, что у нас есть интересные технические возможности, однако как в полной мере реализовать их потенциал, не вполне понятно. Думаю, что в ближайшем будущем мы должны найти ответ на этот вопрос.
Применение лазера должно оградить нас от ошибок и хирургических погрешностей, связанных с человеческим фактором. Однако, по нашему опыту, это не всегда так. На рис. 8 видно, что капсулорексис, выполненный фемтолазером, расположен эксцентрично. Это было связано с тем, что хирург, задавая параметры капсулорексиса, сдвинул его книзу для того, чтобы обойти локальную спайку радужки и передней капсулы хрусталика. Данная потребность, очевидно, возникла в результате операционной ситуации, однако он иллюстрирует то, что лазерный капсулорексис вовсе не идентичен термину «идеальный капсулорексис».
Следующим этапом операции является гидродиссекция. Он в ходе ФЛЭК имеет ряд особенностей. В частности, затруднения связаны с тем, что передние кортикальные массы, расположенные непосредственно под капсулой, подвергаются воздействию лазера. «Спекание» этих слоев затрудняет распространение волны жидкости. Вторая особенность связана с аккумуляцией позади хрусталика пузырьков газа как результата фемтолазерной фрагментации ядра.
С особенной осторожностью мы стали относится к этапу гидродиссекции после публикации австралийских коллег. Они сообщили о синдроме «капсульного блока», который возникал при форсированной гидродиссекции, приводящей к разрыву задней капсулы, и сопровождался дислокацией ядра хрусталика в полость стекловидного тела.
На сегодняшний момент гидродиссекцию мы проводим очень деликатно. По мере плавного введения жидкости контролируем положение пузырьков газа и стараемся их выпустить из ретролентикулярного пространства с целью снижения внутрикапсульного давления. Завершаем данный этап при условии полной ротации ядра, что свидетельствует о полноценном его отделении от капсульной сумки.
Теперь несколько слов о фрагментации ядра при помощи лазера и о том, позволяет ли она снизить травматичность вмешательства в целом? Хотел бы привести клинический пример удаления плотного ядра хрусталика. Предварительно ядро фрагментировали с использованием циркулярных и радиальных паттернов. Несмотря на наличие щелевидных полостей в ткани ядра, хирургу пришлось манипулировать, чтобы разделить его задние слои. Часть ядра не подверглась лазерному воздействию в связи с необходимостью соблюдения так называемой «зоны безопасности». Ее протяженность варьирует от 700 до 1000 микрон кпереди от задней капсулы хрусталика. При мягкой катаракте эпинуклеарные массы, расположенные в этой зоне, достаточно мягкие и не вызывают проблем с расколом ядра. Мы знаем, что при традиционной факоэмульсификации катаракт высокой плотности, задние слои существенно осложняют раскол ядра, затрудняя работу хирургов. К сожалению, пока лазер не дает нам возможности реализовать свои потенциальные преимущества именно в этой критической зоне.