К основным преимуществам операции данного типа можно отнести возможность использования малых самогерметизирующихся разрезов; проведение операции в условиях поддержания стабильной глубины передней камеры и снижение риска грозных интра-операционных осложнений; сведение к минимуму индуцированного астигматизма. Очень важным является сохранение иннервации собственной роговицы, поскольку не проводится ее циркулярная трепанация, вследствие чего также обеспечивается устойчивость глаза к травматическим воздействиям. При необходимости удаления катаракты в ходе ЭК, мы можем точно рассчитать диоптрийность ИОЛ, поскольку послеоперационный астигматизм минимален и форму роговицы в послеоперационном периоде можно достаточно четко прогнозировать. ЗПАК обеспечивает быстрое купирование симптоматики заболевания и скорую зрительную реабилитацию пациента.
Особо стоит отметить возможность применения данной технологии при ранее проведенной сквозной кератопластике, когда существует необходимость замены утраченных эндотелиальных клеток роговичного трансплантата.
По данным Американской ассоциации глазных банков, в последнее десятилетие количество сквозных кератопластик драматически снижается, в то время как количество эндотелиальных кератопластик существенно возрастает. Эту же тенденцию мы отмечаем во всех экономически развитых странах мира.
Основным показанием к операциям замены задних слоев роговицы является эндотелиально-эпителиальная дистрофия. Первичная, как, например, дистрофия Фукса, либо повторная — ЭЭД роговицы при артифакии.
На первом этапе операции ЗАПК под контролем ультразвуковой пахиметрии формируется донорский трансплантат с использованием микрокератома (Мориа, Франция). В зависимости от исходной толщины выполняем 2-3 среза поверхностных слоев роговицы, установленной в специальный держатель — «искусственную» переднюю камеру. Целевой показатель финальной пахиметрии при подготовке ультратонкого трансплантата (120 мик-рон) достигаем путем выбора различных головок микрокератома, обеспечивающих разную глубину реза. Подготовку трансплантата заканчиваем его трепанацией высекателем Barron (Katena, США) нужного диаметра.
И переходим к работе с пациентом. После подготовки операционного поля, производим оценку эпителия и стромы роговицы. При начальных стадиях ЭЭД роговицы их прозрачность, как правило, страдает в минимальной степени, и хирург в процессе операции может визуализировать структуры передней камеры глаза. В противном случае требуется удаление эпителия, что у подавляющего большинства пациентов обеспечивает адекватный визуальный контроль за манипуляциями хирурга. На роговицу наносим разметку, как правило, диаметром 7,0-8,5 мм, в пределах которой будем удалять ДМ. Отделение последней осуществляем в условиях заполнения передней камеры вискоэластиком, для чего используем исключительно когезивные препараты, представляющие собой 1% р-р гиалуроната натрия, например, микровиск (Швеция). Особенность данного класса препаратов в том, что они не адгезируются к тканям глаза и быстро аспирируются из передней камеры. Этап мембранорексиса проводим обратным крючком Sinskey и разработанным нами специальным пинцетом (Titan Surgical, Россия). Вискоэластик вымываем.
Предварительно заготовленный трансплантат, состоящий из задних слоев стромы, ДМ и эндотелия, укладываем в специальную металлическую воронку (Busin глайд) и протягиваем в переднюю камеру пинцетом, введенным в противолежащий основному разрезу парацентез. Накладываем узловой шов (нейлон 10/0) на основной разрез и замещаем физиологический раствор на воздух. После 10-минутной экспозиции воздух почти полностью удаляем и проверяем разрезы на герметичность.
Оперативная техника ЗАПК имеет множество технических вариантов исполнения. Отработанный нами на протяжении ряда лет на нескольких сотнях пациентов и описанный выше вариант операции сопровождается минимальным количеством осложнений и практически гарантирует достижение хорошего анатомического и функционального результата. Последний напрямую связан с минимальной толщиной и равномерностью трансплантата задних слоев роговицы.
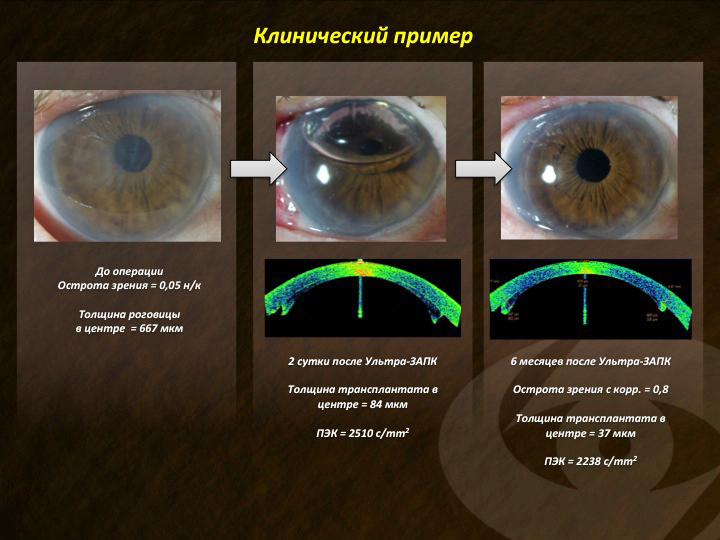
На рис. 17 представлен клинический пример пациента с ЭЭД роговицы. Даны его исходные данные, состояние сразу после операции и в отдаленные сроки.
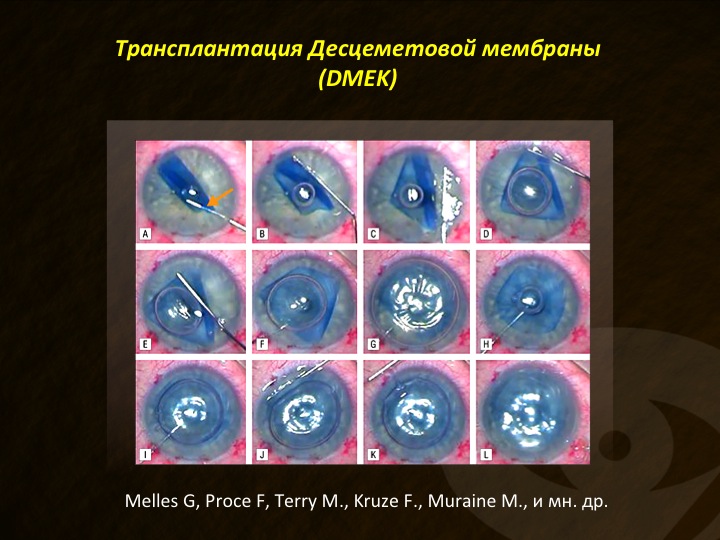
Еще одним направлением эндотелиальной кератопластики, которое считаем обязательным упомянуть, является пересадка десцеметовой мембраны (ПДМ) или согласно международной аббревиатуре — DMEK (Descemet membrane Endothelial Keratoplasty).
Данная операция стремительно завоевывает сторонников во всем мире и несомненно является вершиной эндотелиальной кератопластики не только по получаемому результату, но и по сложности технического исполнения. Особенно значим тот факт, что при пересадке исключительно ДМ с эндотелием, без части стромы, удается снизить частоту отторжений трансплантата. Также важно, что при данной операции количество пациентов, достигающих остроты зрения с коррекцией равной 1,0, много выше, чем при ЗАПК.
Тем не менее у ПДМ есть и существенные недостатки. В первую очередь это касается значительной травмы эндотелия как в ходе подготовки трансплантата, так и при его введении, сопровождаемом расправлением в передней камере. Дело в том, что при отделении ДМ от стромы, она моментально скручивается, принимая форму свитка. Причем эндотелий роговицы оказывается на его внешней поверхности (рис. 18).
Соответственно, любые манипуляции с отделенной мембраной повреждают этот крайне уязвимый клеточный слой. Новые техники ПДМ, например та, что предложена д-ром Марком Мурейном (Франция) и которую мы сейчас активно используем в своей практике, дает возможность существенно снизить вероятность повреждения эндотелиальных клеток при выделении и имплантации ДМ. Есть и ряд других интересных технических решений, направленных на повышение результативности ПДМ, и эти вопросы сейчас находятся в фокусе научных исследований.
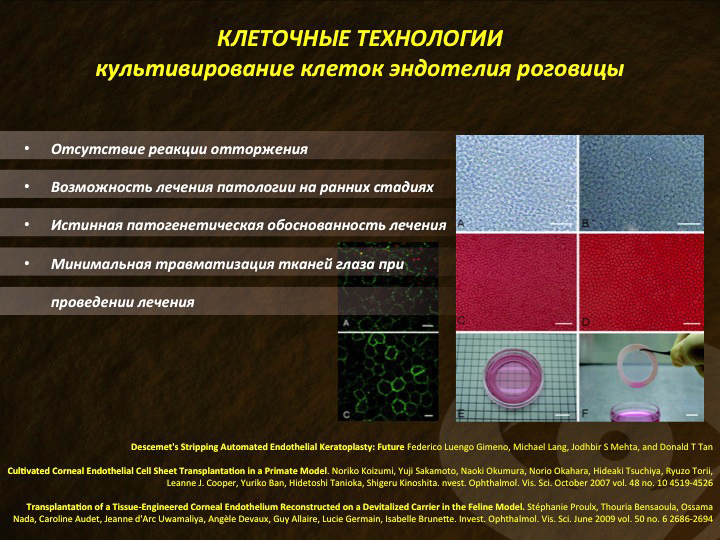
Не меньшее внимание приковано к исследованиям японских офтальмологов. Д-р Шигеру Киношита с коллегами показал возможность использования ингибитора RHO-киназы (ROCK) для лечения дисфункции эндотелия роговицы сначала в эксперименте in vitro, а затем и на приматах. К настоящему моменту уже успешно пролечены 3 пациента с эндотелиальными дистрофиями роговицы (рис. 19).
Исходя из этого, вполне возможно, что ЭЭД роговицы вскоре перестанет быть грозным диагнозом, неотвратимо требующим проведения рано или поздно того или иного вида хирургического вмешательства. Полагаю, что при самых начальных признаках ЭЭД роговицы будут использовать медикаментозную терапию в виде капель или интраокулярного введения препаратов, скорее всего основанных на RНО-киназе, а хирургия останется ведущей при лечении развитых и далеко зашедших стадий заболевания.
Однако это дело будущего, а сегодня мы располагаем великолепными хирургическими технологиями, которые продолжают стремительно развиваться. Для нас, с появлением и внедрением в клиническую практику передней глубокой послойной кератопластики и пересадки десцеметовой мембраны, захватывающей выглядит возможность использовать одну донорскую роговицу для операции сразу двух пациентов. Внедрение данного метода, особенно в наших реалиях ограниченной доступности донорского материала для кератопластики, позволит расширить круг пациентов, которым может быть оказана хирургическая помощь, дав существенные медико-экономический и социальный эффекты. Первый опыт выполнения таких сочетанных селективных трансплантаций фрагментов одной роговицы двум пациентам у нас в МНТК «Микрохирургия глаза» уже есть.